Merupakan lanjutan dari artikel sebelumnya mengenai sifat koloid
Pembuatan Koloid
Larutan Koloid dapat dibuat dengan dua cara :
Dengan Cara Dispersi
jalan Cara Dispersi adalah suatu cara pembuatan larutan koloid dengan mengubah partikel-partikcl kasar menjadi partikel koloid.
Partikel kasar –> Partikel Koloid
Cara dispersi ini dapat dilakukan dengan cara kimia atau cara mekanik
a. Dengan cara Mekanik
Materi yang besar dihaluskan dengan cara menggunakan penggilingan koloid. karbon kasar dijadikan halus lalu didispersikan ke dalam air.
b. Dengan cara Peptisari
Dengan penambahan elektrolit (zat kimia) maka endapan yang terjadi dapat diubah menjadi partikel koloid. Endapan Al(OH)3, terjadi apabila reaksi pembentukan Al(OH)3 dalam jumlah yang banyak. Endapan tersebut dapat berubah menjadi koloid apabila ditambah AlCl3 Jika Gas H2S dialirkan keendapan cas atau endapan NiS akan terbentuk Sol S yang terdispersi. Maka endapan ini membentuk sol sulfida bukan dan larutan.
Dengan Cara Kondensasi
Cara kondensasi dapat dilakukan dengan cara kimia atau dapat dilakukan dengan cara penurunan kelarutan. Atau partikel-partikel diubah menjadi partikel besar yang berukuran koloid. Untuk menurunkan kelautan zat tersebut kita ganti pelantnya. Dalam proses kondensasi, molekul molekul dari larutan direaksikan menghasilkan suatu senyawa
yang sukar larut dalam ni dan membentuk partikel koloid.
Partikel molekuler (kondensasi) —> Partikel koloid
Reaksi kimia yang sering dilakukan untuk menghasilkan partikel koloid dapat dilihat pada contoh berikut ini:
Reaksi Redoks
Pada reaksi berikut terjadi perubahan bilangan oksidasi:
a. Pembuatan sol belerang
sol belerang ini dapat dibuat dengan mengalirkan gas H2S kedalam lantan SO2
2H2S + SO2 –> 3S + 2H2O
b. Pembuatan sol emas
2AuCl3 + 3HCOH + 3H2O –> 2Au + 6HCl + 3HCOOH
AuCl3 + 3FeSO4 –> Au + Fe2(SO4)2 + FeCl3
Reaksi Hidrolisis
a. Dengan penambahan larutan FeCl3 ke dalam air yang sedang mendidih membentuk sol Fe(OH)3, maka reaksi elektrolisa dapat terbentuk sebagai berikut
FeCl3 + 3H2S –>Fe(OH) 3 + 3HCl
b. Sol senyawa hidrolisis yang sukar larut seperti Fe(OH) 3. Al(OH)3 dapat dibuat dari reaksi hidrolisis dengan air.
Contoh:
1. Pembuatan sol Fe(OH)3
Dalam air yang mendidih ditambahkan larutan FeCl3 akan terjadi
FeCl2 +H20 –> Fe(OH)3 + 3HCl
2. Pembuatan sol Al(OH)3
Jika air dimasukan larutan Al(SO4)3, atau AlCl3 (tawas) akan terjadi :
AlCl3 + 3H2O –> Al(OH)3 + 3HCl
3. Reaksi penggaraman
Pada pereaksi yang encer dapat membentuk partikel koloid dari beberapa sol garam yang sukar larut, seperti BaSO4, PbI2, AgCl, PbSO4, AgBr
Contoh
AgNO3 + NaCl –> AgCl + NaNO3
4. Reaksi subtitusi
Dalam larutan asam arsent encer melalui reaksi subtitusi, dialirkan gas H2S membentuk sol As2S3 sebagai berikut.
2H3AsO3 + 3H2S –> As2S3 + 6H20
Dispersi Koloid
Sistim dispersi zat dapat dibedakan menurut ukurannya
1.Dispersi halus
Ukuran partikel-partikel suatu zat yang didispersikan antara 1 sampai dengan 100 millimikron.
2. Dispersi kasar
Partikel partikel zat yang didispersikan lebih dari 100 millimikron.
3. Dispersi molekuler
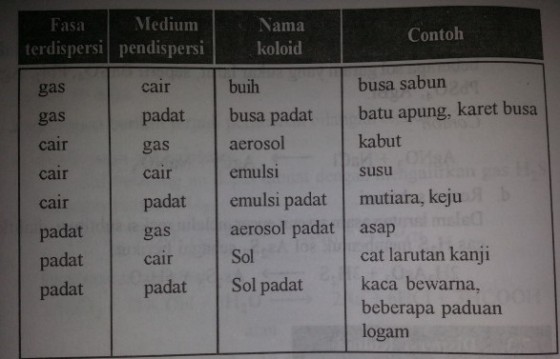
Partikel partikel yang lebih kecil dari pada 1 millimikron merupakan partikel-partikel zat yang didispersikan. Ada beberapa fase dari sistim koloid tersebut, yaitu : fase dispersi dan fase medium dispersi. Kedua fase ini terdapat gas cair dan padat.
Jadi pada kedua fasa tersebut di atas terdapat hubungan sistimkoloid dapat dilihat pada tabel di bawah ini





[…] SILAHKAN MELANJUTKAN KE ARTIKEL BERIKUTNYA MENGENAI KOLOID DI SISTEM KOLOID : PEMBUATAN DAN DISPERSI […]
terimakash NHuey Saangat MembantTu saya
sama sama. Senang bisa membantu 🙂
trims materinya Kata kita blog.s