Rangkuman Kimia Karbon Lengkap
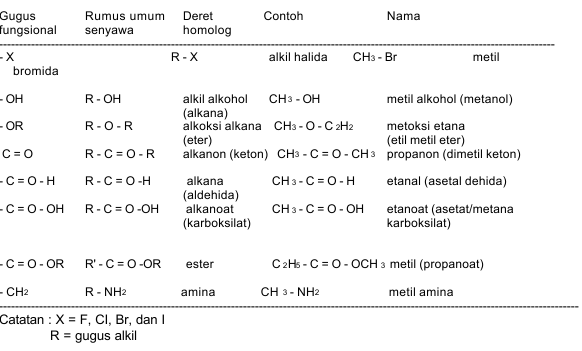
IV. GUGUS FUNGSIONAL DAN REAKSI PENGENALANNYA
A. ALKOHOL
Alkohol (alkohol monovalen) dengan rumus umum R – OH dapat dianggap sebagai turunan dari hidroksil suatu alkana atau turunan alkil dari air.
Pembagian alkohol:
a. Berdasarkan letak gugus OH pada rantai karbon.
Alkohol dibagi menjadi 3 macam yaitu :
1. Alkohol Primer ialah alkohol yang gugus OH-nya terikat pada atom C primer.
Atom C primer ialah atom C yang terikat pada satu atom C yang lain.
2. Alkohol Sekunder ialah alkohol yang gugus OH-nya terikat pada atom C sekunder.
Atom C sekunder ialah atom C yang terikat pada dua atom C yang lain.
3. Alkohol Tersier
Alkohol tersier ialah alkohol yang gugus OH-nya terikat pada atom C tersier.
Atom C sekunder ialah atom C yang terikat pada tiga atom C yang lain.
b. Berdasarkan banyak gugus -OH yang terikat pada rantai C.
Alkohol dibedakan atas :
1. Alkohol Monovalen disebut juga alkanol yaitu alkohol yang hanya memiliki satu gugus OH.
2. Alkohol Polivalen yaitu alkohol yang memiliki gugus -OH lebih dari satu.
Jika memiliki 2 gugus OH dinamakan alkandiol.
Jika memiliki 3 gugus OH dinamakan alkantriol dan seterusnya.
Isometri pada alkohol terjadi karena :
1. Letak gugus OH-nya.
2. Ada/tidak ada cabang
3. Letak cabang-cabangnya.
Pembuatan:
Alkohol dapat dibuat dengan beberapa cara :
1. Mereaksikan alkil halida dengan KOH atau AgOH (suspensi Ag2O dalam eter berair) dalam air.
2. Mereaksikan amina primer dengan asam nitrit.
3. Reduksi senyawa karbonil ialah senyawa yang mengandung gugus C = O.
• reduksi alkanal mengahsilkan alkohol primer
• reduksi alkanon menghasilkan alkohol sekunder.
4. Sintesis Grignard
Senyawa Grignard (alkil magnesium kalida) sangat penting dalam pembuatan berbagai
macam alkohol. Pada reaksi ini terjadi adesi RMgX pada gugus karbonil dengan
hidrolisis.
B. ETER
Eter merupakan senyawa karbon turunan alkana, satu atom H dari alkana diganti
dengan gugus alkoksi (-O – R), sehingga eter dinyatakan dengan :
Rumus umum: R – O – R’
Isomerisasi
Isomerisasi pada eter disebabkan karena letak gugs fungsional – O R -nya atau cabang-abangnya.
Eter selain berisomer sesamanya juga berisomer dengan alkohol (isomer fungsional).
Pembuatan eter
Eter dapat dibuat dengan cara :
1. Eliminasi Alkohol
Pada cara ini campuran alkohol dan asam sulfat pekat dipanaskan sampai 140oC. Asam sulfat pekat selain sebagai katalisator juag sebgai zat hidroskopis.
2. Sintesis William son
Pada cara ini alkil halida direaksikan dengan natrium alkoholat
Kegunaan eter
• Sebagai pelarut senyawa-senyawa organik
• Sebagai obat bius pada pembedahan.
C. ALDEHIDA/ALKANAL
Aldehida/alkanal dianggap sebagai turunan alkana di mana 1 atom H dari alkana diganti dengan gugus fungsional – C = O – O sehingga aldehida/alkanal ditulis dengan rumus umum R – C = O – H
Isomerisasi pada alkanal terjadi karena adanya cabang dan letak cabang.
Selain alkanal berisomer sesamanya juga berisomer dengan alkanon (isomeri fungsional).
Pembuatan Alkalna dapat dibuat dengan beberapa cara, diantaranya :
1. Mengoksidasi alkohol primer
Sebagai oksidator dapat digunakan oksigen dari udara, asalkan menggunakan katalis platina atau tembaga.
2. Memanaskan campuran natrium karboksilat dan natrium format kering. (destilasi kering)
3. Mereaksikan alkil ester asam format dngan senyawa Grignard.Metanal (H – C = O – H)
Metanal merupakan suku pertama deret homolog aldehida, pada suhu kamar berwujud gas tak berwarna berbau rangsang. Larutan metanal 40% dalam air diperdagangkan dengan nama formalin. Formalin ini digunakan untuk mengawetkan benda-benda
anatomi. Metanal banyak digunakan sebagai bahan baku untukk pembuatan zat warna, plastik dan lain-lain.
Pembuatan :
1. Oksidasi metanol dengan oksigen dari udara dengan menggunakan Cu sebagai katalis.
2. Reduksi gas CO oleh H 2 .
D. ALKANON (KETON)
Alkanon ialah senyawa yang dianggap turunan hidrokarbon dengan gugus fungsional
C = O (gugus karbonil)
yang dinyatakan dengan rumus umum :
O
II
R – C – R’
Isomerisasi pada alkanon disebabkan oleh:
- ada/tidaknya cabang serta letak cabang
- letak gugus fungsionalnya.
Selain alkanon berisomer sesamanya, juga berisomer dengan alkanal (isomer fungsional).
Pembuatan
Alkanon dapat dibuat dengan berbagai cara :
1. Mengoksidasi alkohol sekunder
ROH – CH – R’ + O2 → RO – C – R’ + H2O
- Distilasi kering garam-garam alkali/alkali tanah karboksilat.
Aseton (propanon)
Aseton merupakan suku alkanon yang tendah. Pada suhu kamar aseton berupa zat cair tak berwarna, mudah menguap, mudah terbakar berbau manis dan mudah larut dalam air.
Aseton digunakan sebagai pelarut senyawa-aenyawa organik, teritama untuk melarutkan beberapa macam plastik dan gaas etena. Aseton juga digunakan untuk membuat klorofom dan yodoform.
Pembuatan Secara besar-besaran aseton dapat dibuat dengan distilasi kering kalsium asetat.
E. ASAM KARBOKSILAT (ALKANOAT)
Alkanoat atau asam kalboksilat adalah turunan dari alkana,jika satu atom H dari alkana
diganti dengan gugus fungsional – C = O – OH Sehingga rumus umum alkanoat dinyatakan dengan R – C = O – OH
Alkanoat disebut juga sebagai asam lemak, karena asam-asam ini banyak terdapat di alam sebagai lemak (dalam bentuk ester dengan alkohol)
Isomerisasi pada alkanoat disebabkan karena ada/tidaknya cabang serta letak cabang- cabangnya. Alkanoat selain berisomer sesamanya juga berisomer dengan ester (dibicarakan pada ester).
Pembuatan
Reaksi karboksilat dapat dibuat dengan beberapa cara, di antaranya :
1. Oksidasi alkohol primer atau alkanal sebagai oksidator dapat diguankan oksigen di udara, kalium permanganat atau kaliumbikromat dalam suatu asam sulfat.
2. mereaksikan gas CO 2 dengan pereaksi Grignard
3. Sintesis Nitril
Mereaksikan alkil halida dengan NaCN atau KCN dalam larutan beralkohol membentuk alkana nitril (alkil sianida), alkana nitril ini dalam suasana asam/basa terhidrolisis membentuk asam karbonat.
Alkandioat/asam dikarboksilat
Alkandioat adalah asam karboksialt yang mengandung 2 gugus karboksilat.
Asam hidroksi karboksilat
Senyawa golongan ini selain mengnadung gugus karboksilat
- C = O – OH
juga mengandung gugus hidroksil (-OH). Jadi senyawa ini dapat bersifat sebagai asam juga bersifat sebagai alkohol.
Berdasarkan banyaknya gugus -C = O – OH dalam senyawa ini dibedakan :
a. Asam hidroksi monovalen
Asam ini hanya memiliki satu gugus – C = O – OH
b. Asam hidroksi bivalen
Asam ini mengandung dua gugus C = O – OH
c. Asam hidroksi trivalen
Asam ini mengandung tiga gugus C = O – OH
F. ESTER
Ester adalah senyawa karbon turunan asam karboksilat, jika atom H dari gugus fungsional C = O – OH diganti dengan gugus alkil.
Ester dinyatakan dengan rumus umum :
R – C = O – OR’
Isomerisasi pada Ester ditentukan oleh :
1. rantai C pada asam/alkilnya
2. cabang-cabangnya
Selain ester berisomer sesamanya, ester juga berisomer fungsional dengan asam karboksilat.
Pembuatan
Ester dapat dibuat dengan jalan :
1. Mereaksikan asam karboksilat dengan alkohol (esterifikasi fisher) dalam suasana asam.
Reaksinya : R – C = O – OH + R’ – OH ↔ R – C = O – OR’ + H 2 O
Reaksi ini merupakan reaksi kesetimbangan.
2. Mereaksi perak karboksilat dengan alkil halida.
Rumus : R – C = O – OAg + R’ – X → R – C = O – OR’ + AgX↓
3. Mereaksikan anhidrida asam alkanoat dengan alkohol.
4. Mereaksikan halogen asam alkanoat dengan alkohol.
G. AMINA
Alkil amina adalah senyawa karbon turunan amoniak jika satu atau lebih atom H -nya diganti dengan gugus alkil. Dengan demikian amina dibagi menjadi tiga macam, yaitu :
1. “Amina primer” , jika satu atom H dari NH 3 diganti dengan gugus alkil. Rumus amina primer ditulis R – NH 2
2. “Amina sekunder”, jika dua atom H dari NH 3 diganti dengan gugus alkil.
Rumus amina sekunder ditulis R – NH – R’
3. “Amina tersier”, jika tiga atom H dari NH 3 diganti dengan gugus alkil.
Rumus amina tersier ditulis
R – N – R”
I
R’
Senyawa amina (baik itu amina primer,sekunder maupun tersier) mempunyai rumus
umum : CnH2n+3N,dengan n adalah jumlah atom C.
Pembuatan
Amina dibuat dengan cara :
• Mereaksikan alkil halida dengan amonia (alkilasi Hoffman).
Isomerisasi pada amina ditentukan oleh:
1. Rantai C -nya (bercabang/tidak)
2. Letak N -nya
3. Macam aminanya (primer, sekunder atau tersier)
Untuk penjelasan lengkap isomerisasi silahkan lanjut ke halaman 5
- Latihan Soal OSN Ilmu Komputer SMA 2026 - June 1, 2026
- Latihan Soal OSN Kebumian SMA 2026 - May 31, 2026
- Latihan Soal OSN Geografi SMA 2026 - May 30, 2026



2 comments