Materi Pelajaran
Praktikum Kimia
aas, aes, alat kimia, atom, atom atom, atomic absorption spectroscopy, bagan aas, eksitasi elektron, energi, instrument kimia, kimia universitas, larutan, pembahasan AAS, praktikum kimia, radiasi, spektroskopi, spektroskopi emisi, ssa, tingkat
Krisna Dwi Wardhana
2 Comments
Pembahasan AAS atau SPEKTROSKOPI SERAPAN ATOM
SPEKTROSKOPI SERAPAN ATOM
Pendahuluan
Spektroskopi atom digunakan untuk mengidentifikasi dan menentukan (kualitatif dan kuantitatif) logam-logam dalam tingkat ‘trace” dalam semua jenis materi dan larutan. Pengukuran dalam spektroskopi serapan atom (SSA) berdasarkan radiasi yang diserap oleh atom yang tidak tereksitasi dalam bentuk uap. Dalam spektroskopi emisi, pengukuran berdasarkan energi yang diemisikan ketika atom atom dalam keadaan tereksitasi untuk kembali ke keadaan dasar. Spektroskopi Emisi Nyala (SEN) adalah suatu spektroskopi emisi dari daerah khusus yang mana atom dieksitasi dengan menggunakan nyala. Pada Gambar : 1 di bawah ini menggambarkan proses serapan dan emisi.
Gambar 1. Hubungan antara spektroskopi emisi dan serapan atom.
Teknik serapan dan emisi nyala biasanya disertai pemasukkan suatu larutan sampel bentuk aerosol dalam nyala. Evaporasi pelarut dan penguapan garam terjadi terlebih dahulu untuk mendisosiasi garam ke dalam atom atom gas yang bebas. Pada suhu nyala udara-asetilen (± 2300oC) atom dari sejumlah banyak unsur berada dalam keadaan dasar. Jika seberkas energi radiasi yang terdiri dari spektrum emisi untuk unsur tertentu yang akan ditentukan dilewatkan melalui nyala ini, sejumlah atom dalam keadaan dasar akan menyerap energi dari panjang gelombang yang karakteristik (garis resonansi) dan mencapai keadaan energi yang lebih tinggi.
Jumlah energi radiasi yang diserap sebagai suatu fungsi konsentrasi unsur dalam nyala merupakan dasar spektroskopi serapan atom. Untuk beberapa unsur seperti logam alkali, Na dan K, nyala udara-asetilen cukup panas tidak hanya menghasilkan atom atom dalam keadaan dasar, tetapi juga menaikkan sejumlah atom ke keadaan elektronik tereksitasi. Energi radiasi dipancarkan (diemisikan) jika atom-atom kembali ke keadaan dasar yang sebanding dengan konsentrasi dan merupakan dasar spektroskopi emisi nyala.
Contoh pada 589,0 nm emisi nyala
Pancaran/emisi energi radiasi dari emisi nyala atau energi radiasi lampu eksternal yang tidak bisa hilang oleh serapan atom akan didispersi oleh monokromator dan dideteksi oleh fotomultiplier. Pada energi yang lebih tinggi fraksi atom atom keadaan dasar ada sebagian yang tereksitasi, sebagai dirumuskan oleh persamaan Boltzman sebagai berikut :
k = tetapan Boltzman
T = suhu nyala Kelvin
Ej = perbedaan energi dalam energi dari tingkat tereksitasi dasar
Nj = jumlah atom pada tingkat tereksitasi
No = jumlah atom pada tingkat dasar
Pj dan Po = faktor statistik yang ditentukan oleh jumlah tingkat yang mempunyai energi yang sama dari atom yang tereksitasi dan pada tingkat dasar.
Suatu sampel pertama-tama harus dilarutkan, proses pelarutan dikenal dengan istilah destruksi, yang bertujuan untuk membuat unsur logam menjadi ion logam yang bebas. Terdapat dua cara destruksi yaitu :
- Destruksi basah : sampel ditambahkan asam asam oksidator, jika perlu dibantu dengan pemanasan.
- Destruksi kering: sampel langsung dipanaskan untuk diabukan.
Hasil destruksi baik cara basah maupun kering kemudian dilarutkan Larutan sampel dimasukkan ke dalam nyala dalam bentuk aerosol yang selanjutnya akan membentuk atom atomnya. Serapan akan terjadi dari radiasi suatu sumber sinar yang sesuai dengan atom yang akan ditentukan. Sebagai sumber emisi sinar adalah lampu katoda berongga yang mempunyai garis spektra yang tajam.
Metode analisis ini bersifat cepat, selektif, sensitif dan mempunyai akurasi yang tinggi serta dapat digunakan secara rutin. Di dalam spektroskopi serapan atom dijumpai adanya beberapa gangguan yang dapat mempengaruhi keakuratan atau kesalahan pengukuran. Pada dasarnya terdapat 3 tipe gangguan, yaitu :
- gangguan fisika
- gangguan kimia
- gangguan spektral
Gangguan fisika dan kimia dalam nyala akan mengubah populasi atom, sedangkan gangguan spektral akan mempengaruhi pengukuran yang sebenarnya dari serapan atom. Pengaruh gangguan ini dapat dikurangi atau dihilangkan dengan cara menseleksi kondisi percobaan atau dengan memberi perlakuan kimiawi pada sampel yang sesuai dengan permasalahannya. Demikian pula untuk mengatasi gangguan spektral yaitu dengan cara memisahkan unsur-unsur yang mengganggu.
Sesuai dengan tujuan dan fungsi nyala yang sesuai dengan suhu atomisasi suatu unsur, maka terdapat beberapa komposisi nyala seperti :
– argon-hidrogen : maksimum temperatur 1577o C
– hidrogen-udara : maksimum temperatur 2045o C
– udara-asetilen : maksimum temperatur 2300o C
– dinitrogen oksida-asetilen : maksimum temperatur 2955o C
Berikut bagan alat spektroskopi serapan atom sistem berkas tunggal .
Gambar : 2. Prinsip peralatan AAS
————————————————————————–
PERCOBAAN
Prinsip operasi metode ini yaitu diperlukan sumber cahaya dari luar yang memancarkan sinar dengan panjang gelombang tertentu, yang sesuai dengan energi yang diperlukan untuk mengubah tingkat energi elektronik dari tingkat dasar ke tingkat eksitasi suatu unsur. Sinar dengan panjang gelombang yang diperlukan ini dilewatkan nyala yang mengandung unsur yang akan diukur. Perbedaan antara intensitas sinar mula-mula dengan intensitas sinar yang diteruskan diukur dan perbedaan ini sebagai nilai absorban dan besarnya berbanding lurus dengan konsentrasi unsur yang mengabsorpsi sinar tersebut.
Beberapa percobaan ini merupakan usaha untuk memahami hal-hal sebagai berikut : 1. Pembuatan kurva kalibrasi
- Mencari dan menentukan batas deteksi
- Mempelajari beberapa sifat gangguan dan cara mengatasinya
- Mencari kondisi optimum seperti :
– kecepatan gas pembakar
– kecepatan gas oksidan
– tinggi burner head
- Menentukan kadar sesuatu unsur.
- Pembuatan Kurva Kalibrasi Fe dan penentuan Fe dalam air buangan/air minum
Ferrum dapat ditentukan dalam nyala udara-asetilen. Nyala udara-asetilen memberikan suhu yang sesuai dengan suhu yang diperlukan untuk atomisasi logam Fe. Untuk menentukan kandungan Fe dalam air minum atau air buangan, diperlukan perlakuan yang sama antara larutan standar logam Fe dengan sampel.
Cara kerja :
Preparasi larutan standar
– Buatlah larutan standar baku Fe 1000 ppm, dari larutan standar baku tersebut buatlah seri larutan standar 0,1 hingga 5 ppm. Pada pembuatan larutan standar tambahkan asam HNO3 pekat beberapa tetes atau HCl pekat beberapa tetes, selanjutnya encerkan sesuai dengan volume labu ukur (gunakan labu ukur 100 ml).
Penyiapan sampel :
– Ambil sejumlah volume air buangan/minum, saring dengan kertas saring Whatman nomor 42, beri beberapa tetes HNO3 pekat, tempatkan dalam labu ukur 100 ml.
Alat :
– Spektrometer Serapan Atom
– Kertas saring Whatman nomor 42
– Labu ukur 100 ml (10 buah), 250 ml (2 buah),
– corong pendek
– pipet ukur, dll.
Bahan Kimia :
– Asam HNO3 dan HCl pekat.
Cara Pengukuran :
– Perhatikan prosedur pengoperasian alat spektrometer serapan atom (ikuti petunjuk instruktur)
– Tentukan dan ukur larutan standar beserta larutan sampel.
– Buatlah kurva kalibrasi, secara grafik dan dengan metode “least-square” persamaan linier, tentukan harga koefisien korelasi.
– Buatlah batas deteksi alat terhadap unsur Fe, catatlah kondisi operasi alat.
– Hitung besarnya kandungan Fe dalam air buangan atau air minum.
Pertanyaan :
Dapatkah untuk analisis logam Fe dipakai nyala N2O-asetilen ? Terangkan jawaban saudara!
- Analisis Tanaman (Sayuran), untuk unsur Ca, Cu, Fe, Mg, Mn, K dan Zn.
Alat : – Spektrometer serapan atom
– Labu ukur 250 (2 buah), 100 ml (4 buah) dan 50 ml (10 buah)
– Pipet ukur dan pipet tetes.
– Labu erlenmeyer 100 ml (5 buah) berserta corong pendek kecil.
– Alat pemanas (hot plate)
– Botol timbang
– Alat neraca elektronik.
Bahan Kimia : – HNO3 pekat, HCl pekat, HClO4 pekat, H2O2 30%.
Cara Pengerjaan :
Preparasi Sampel dan larutan standar
- Untuk konstituen mineral :
Pisahkan dengan hati-hati semua materi asing, khususnya tanah dan pasir yang melekat, tetapi cegah adanya “leaching”, hindari pencucian yang terus menerus. Gunakan udara atau oven pengering secepat mungkin untuk mencegah dekomposisi atau hilangnya berat oleh respirasi, haluskan dan simpan dalam botol tertutup. Jika hasil diharapkan yang berasal dari berat segar, catat berat sampel sebelum dan sesudah pengeringan.
- Teknik Pengabuan (dry ashing) :
Timbang 1 g sampel, keringkan dan haluskan, gunakan atau masukkan ke dalam krusibel porselin. Abukan selama 2 jam pada suhu 500oC. Dinginkan, tambahkan 10 tetes H2O dan secara hati-hati tambah 3-4 ml HNO3 (1:1), uapkan kelebihan HNO3 pada pemanas pada suhu 100-120oC. Kembali krusibel dipanaskan dalam tungku pemanas (furnace) selama 1 jam pada suhu 500°C. Dinginkan, larutkan abu dalam 10 ml HCl (1:1) dan pindahkan ke dalam labu ukur 50 ml, tambahkan H2O hingga batas, larutan siap diukur.
- Teknik destruksi basah (wet ashing) :
Timbang dengan baik sekitar 1 g sampel, keringkan dan haluskan kemudian masukkan ke dalam labu Erlenmeyer 50 ml, tambahkan 10 ml HNO3 pekat, kocok dengan hati-hati, tambahkan 3 ml HClO4 60% dan panaskan pada hot plate (dalam lemari asam) perlahan-lahan, hingga busa berhenti. Panaskan lebih lanjut hingga HNO3 hampir menguap semua. Jika terjadi arang dinginkan dan tambahkan 10 ml HNO3 pekat lagi dan lanjutkan pemanasan. Panaskan hingga terbentuk asap putih dari HClO4. Dinginkan dan tambah 10 ml HCl (1:1) dan pindahkan ke dalam labu ukur 50 ml. Larutan siap dianalisis.
- Siapkan larutan standar sesuai dengan jenis unsur yang akan ditentukan.
Untuk seri bagi unsur : Fe, Cu, Mn dan Zn dari 1,0 – 10,0 ppm
Untuk seri bagi unsur : Ca, Mg, dan K dari 0,1 – 5,0 ppm.
Cara Pengukuran :
- Persiapkan pengoperasian alat (petunjuk instruktur)
- Ukur serapan larutan standar dan larutan sampel dalam satu kondisi.
- Buatlah kurva kalibrasi dengan metode “least squarre”, koefisien korelasi.
- Tentukan batas deteksi alat terhadap unsur melalui larutan standar.
- Hitunglah kandungan unsur dalam sampel.
Daftar Pustaka :
- Buku Panduan Praktikum Instrumen Dep. of Anal. Chem, NSW., 1979.
- Willert, Marritt dan Dean, “Anal. Chem.”, 1979.
- A.O.A.C., Plant Analysis : 3.002(a), 3.006; 3.007; 3.007; 3.008 dan 2.109-2.110.
- Chemistry Experiments : AA and AE Spectroscopy, John Wiley Sons, 1984.
Latest posts by Krisna Dwi Wardhana (see all)
- Latihan Soal OSN Kebumian SMA 2026 - May 31, 2026
- Latihan Soal OSN Geografi SMA 2026 - May 30, 2026
- Latihan Soal OSN Ekonomi SMA 2026 - May 29, 2026



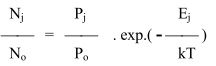




2 comments