Materi Pelajaran
berkeley national laboratory, Biochemistry and Molecular Biology, Biology, Biomolecules, DNA, lawrence berkeley national laboratory, Online Services, polar nonpolar, protein, protein structures, Proteins and Enzymes, RNA, sel makhluk hidup, sel manusia
Krisna Dwi Wardhana
0 Comments
Kelarutan Protein
Protein adalah senyawa organik kompleks dan merupakan polimer dari monomer-monomer asam amino yang dihubungkan satu sama lain dengan ikatan peptida. Molekul protein mengandung karbon, oksigen, hidrogen,
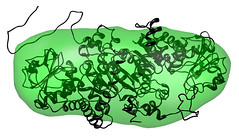
nitrogen, dan kadang kala sulfur serta fosfor. Protein berperan penting dalam struktur dan fungsi semua sel makhluk hidup dan virus. Kebanyakan protein merupakan enzim atau subunit enzim. Protein merupakan salah satu dari biomolekul raksasa, selain polisakarida, lipid, dan polinukleotida, yang merupakan penyusun utama makhluk hidup. Selain itu, protein merupakan salah satu molekul yang paling banyak diteliti dalam biokimia. Protein ditemukan oleh Jöns Jakob Berzelius pada tahun 1838 (Abrams, 2010).
Ada 20 asam amino yang memiliki perbedaan pada struktur rantai samping telah digunakan sel-sel manusia untuk membuat protein. Struktur rantai samping menentukan kelas-kelas asam amino, antara lain seperti polar, nonpolar, netral, asam, dan basa. Sel manusia dapat mensintesis kebanyakan asam amino yang dibutuhkan untuk membuat protein. Meskipun begitu ada sekitar delapan asam amino yang disebut sebagai asam amino esensial karena tidak dapat disintesis oleh sel manusia sehingga harus didapatkan dari makanan (Goff, 1995).
Asam amino tergabung dengan ikatan kovalen oleh ikatan peptida menjadi protein. Ikatan peptida merupakan ikatan amida yang dibentuk antara ikatan asam karboksilat asam amino satu dengan gugus amina asam amino yang lain. Setiap asam amino mengandung paling tidak satu gugus amina dan satu gugus asam karboksilat. Dapat juga terbentuk ikatan peptida dengan dua cara. Contohnya seperti yang terjadi pada Gambar 2 dan juga mungkin terjadi ikatan peptida antara gugus asam karboksilat valin dengan gugus amina glisin sehinga menghasilkan valilglisin. Sedangkan protein terbentuk dari ratusan asam amino yang dihubungkan dengan ikatan peptida membentuk rantai peptida (Abrams, 2010).
Berikut ini akan ditulis bagaimana protein dapat berionisasi sehingga menjadi dapat bermuatan positif maupun negatif. Prinsip ini adalah prinsip dasar isolasi protein menggunakan garam konsentrasi rendah maupun dengan pengaturan pH pada titik isoelektriknya. Seperti halnya asam amino, protein yang larut dalam air akan membentuk ion yang mempunyai muatan positif dan negatif. Dalam suasana asam molekul protein akan membentuk ion positif, sedangkan dalam suasana basa akan membentuk ion negatif. Pada titik isoelektrik protein mempunyai muatan positif dan negatif yang sama, sehingga tidak bergerak kearah elektroda positif maupun negatif apabila ditempatkan di antara kedua elektroda tersebut. Ionisasi protein dapat digambarkan sebagai berikut (Murray, 2006):
Protein (sebagai kation) <======> H+ + “Protein” (zwitter ion)
NH2– + “Protein” (zwitter ion) <======> Protein (anion)
Protein mempunyai titik isoelektrik yang berbeda-beda. Titik isoelektrik protein mempunyai arti penting karena pada umumnya sifat fisika dan kimia erat hubungannya dengan pH isoelektrik ini. Pada pH di atas titik isoelektrik protein bermuatan negatif, sedangkan di bawah titik isoelektrik protein bermuatan positif (Murray, 2006). Inilah prinsip dari zwitter ion itu sendiri.
Presipitasi protein adalah pengendapan yang terjadi karena penggumpalan yang parsial. presipitasi disebabkan oleh berkurangnya kelarutan protein (perubahan fisik) yang terjadi karean perubahan kimia. Seperti halnya denaturasi protein, presipitasi juga disebabkan oleh factor kimia dan fisika. Semua faktor yang terjadi pada denaturasi juga terjadi pada presipitasi protein. Semua faktor yang dapat menimbulkan denaturasi protein, juga dapat menyebabkan perubahan kelarutan protein. Dengan demikian presipitasi protein merupakan fenomena fisika yang disebabkan oleh perubahan struktur kimia. Presipitasi disebabkan oleh pengembangan molekul protein akibat unfolding atau membukanya heliks-heliks protein. Presipitasi juga terjadi akibat terganggunya kesetabilan koloid yang disebabkan oleh menurunnya muatan elektrostatik protein sehingga gaya gravitasi akan lebih dominan dibandingkan gaya tolak-menolak antar molekul. Kesimpulannya adalah presipitasi protein merupakan fenomena berkurangnya kelarutan suatu protein yang disebabkan oleh perubahan struktur kimia (Genius, 2010).
Metode Salting-in dilakukan dengan menambahkan garam yang tidak jenuh atau pada konsentrasi rendah sehingga protein menjadi bermuatan dan larut dalam larutan garam. Kelarutan protein akan terus meningkat sejalan dengan peningkatan konsentrasi garam, apabila konsentrasi garam ditingkatkan terus, maka kelarutan protein akan turun, pada konsentrasi garam yang lebih tinggi,protein akan mengendap (Genius, 2010).
Pengendapan pada metode salting-out terjadi karena proses persaingan antara garam dan protein untuk mengikat air. Grup ion pada permukaan protein menarik banyak molekul air dan berikatan dengan sangat kuat. Contohnya Amonium sulfat yang ditambahkan ke dalam larutan protein akan menyebabkan tertariknya molekul air oleh ion garam. Hal tersebut disebabkan ion garam memiliki densitas muatan yang lebih besar dibandingkan protein. Kekuatan ionic garam pada konsentrasi tinggi semakin kuat sehingga garam dapat lebih mengikat molekul air. Menurunnya jumlah air yang terikat pada protein menyebabkan gaya tarik menarik antara molekul protein lebih kuat bila dibandingkan dengan gaya tarik menarik anatara molekul protein dan air (mempertinggi interaksi hidrofobik), sehingga protein akan mengendap dari larutan atau berikatan dengan kolom hidrofobik. Selama proses salting-out, konsentrasi garam harus tetap dijaga agar tidak menurun dalam larutan sehingga tidak terjadi pengendapan yang bersamaan antara protein yang ingin dimumikan dan protein yang tidak diinginkan (Genius, 2010). Adapun tujuan dari presipitasi protein biasanya adalah untuk memurnikan, mengkonsentratkan, atau bisa juga apabila protein sebagai pengotor maka dapat dipisahkan dari zat yang diinginkan (Genius, 2010).
Pustaka:
Abrams, Jolane. 2010. DNA, RNA, and Protein: Life at its simplest. Tersedia : http://www.postmodern.com/~jka/rnaworld/nfrna/nf-rnadefed.html.
Genius. 2010. Tersedia: http://farisnh.com/2010/04/imunohistokimia-imunohistokimia_16.html.
Goff, Douglas. 1995. Dairy Chemistry and Physics. Tersedia : http://www.foodsci.uoguelph.ca/dairyedu/chem.html.
Murray, Robert K. 2006. Biokimia Harper. Penerbit Buku Kedokteran EGC: Jakarta
Latest posts by Krisna Dwi Wardhana (see all)
- Latihan Soal OSN Ilmu Komputer SMA 2026 - June 1, 2026
- Latihan Soal OSN Kebumian SMA 2026 - May 31, 2026
- Latihan Soal OSN Geografi SMA 2026 - May 30, 2026



Leave a Reply