Materi Pelajaran
asam alkanoat, asam asetat, asam butirat, asam cuka, asam format, asam karboksilat, asam propanoat, asam semut, asam sitrat, butana, carboxylic acid structure, cnh2no2, ester, formica rufa, gugus, harum, IUPAC, metana, nata de coco, penetralan, pengawet, pengesteran, rantai
Krisna Dwi Wardhana
2 Comments
Senyawa Turunan Alkana: Asam Karboksilat
Asam karboksilat atau disebut juga sebagai asam alkanoat adalah senyawa turunan alkana dengan gugus fungsi
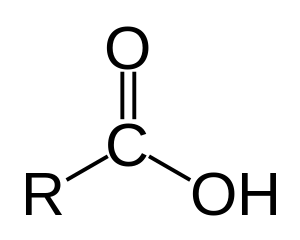
–COOH dan rumus umum CnH2nO2. Asam karboksilat ini termasuk dalam golongan asam organik dan merupakan asam lemah. Secara IUPAC (International Union of Pure and Applied Chemistry), penamaan asam karboksilat dilakukan dengan mengganti akhiran –a dari alkana menjadi –oat dan menambahkan awalan asam. Contohnya adalah alkana menjadi asam alkanoat, metana menjadi asam metanoat, dan butana menjadi asam butanoat. Secara umum, penamaan asam karboksilat didasarkan pada sumber alami asam tersebut. Contohnya adalah asam metanoat disebut sebagai asam formiat (asam format) atau asam semut. Hal ini dikarenakan asam metanoat ditemukan pada semut Formica rufa. Sedangkan contoh lain adalah asam butanoat yang disebut sebagai asam butirat karena ditemukan pada mentega (butter). Asam etanoat disebut sebagai asam asetat karena ditemukan pada cuka (asetum = cuka dalam bahasa Latin).
Adapun rumusan penentuan tata nama asam karboksilat:
- Rantai induk adalah rantai terpanjang yang mengandung gugus fungsi
- Penomoran dimulai dari gugus fungsi (-COOH)
Rumus penentuan tata nama asam karboksilat secara umum adalah:
(no.cabang) (nama cabang dan gugus lain) (nama rantai induk)
Contoh:
CH3-COOH: asam etanoat = asam metana karboksilat = asam asetat = asam cuka
CH3-CH2-COOH: asam propanoat = asam etana karboksilat = asam propionat
CH3-CH2-CH2-COOH: asam 3-metil butanoat = asam 2-metil-1-propana karboksilat = asam isopentanoat = asam isovalerat
Asam karboksilat memiliki beberapa sifat khusus, yaitu:
1. Sifat Fisis
- Titik didihnya cukup tinggi karena adanya ikatan hidrogen dengan berat molekul yang besar
- Memiliki nilai pKa (tetapan asam) kecil
2. Sifat Kimia
- Dapat mengalami reaksi penetralan
- Dapat mengalami reaksi pengesteran
Reaksi-reaksi senyawa asam karboksilat:
1. Penetralan
Asam karboksilat dapat bereaksi dengan basa membentuk garam dan air. Garam natrium atau kalium dari asam karboksilat dikenal sebagai sabun, dimana sabun natrium disebut sebagai sabun keras (contohnya natrium stearat NaC17H35COO), dan sabun kalium disebut sebagai sabun lunak (contohnya kalium stearat KC17H35COO). Larutan garam natrium dan kalium ini dapat mengalami hidrolisis parsial dan memiliki sifat basa. Adapun reaksinya adalah:
CH3COOH + NaOH → NaCH3COO + H2O
2. Pengesteran
Asam karboksilat dapat bereaksi dengan alkohol membentuk ester. Ester adalah suatu senyawa turunan alkana yang memiliki bau harum. Contoh reaksi pengesteran adalah dengan menambahkan etanol dan asam sulfat pekat ke dalam asam asetat.
Kegunaan asam karboksilat:
- Asam format / asam semut
Asam format banyak digunakan dalam industri tekstil, penyamakan kulit, dan perkebunan karet untuk menggumpalkan lateks. Asam format memiliki karakteristik tidak berwarna, berbau tajam, mudah larut dalam air, alkohol, dan eter. Asam format dapat mereduksi perak nitrat dalam suasana netral.
- Asam asetat / asam cuka
Dapat digunakan untuk bahan masakan dalam kadar 20-25%. Asam asetat juga merupakan salah satu bahan baku pembuatan nata de coco.
- Asam sitrat
Asam sitrat digunakan untuk pengawet, contohnya untuk pengawet buah kaleng.
Sumber:
Michael Purba (“Kimia Untuk SMA Kelas XII”)
Richard C. Banks – Nomenclature of Carboxylic Acid (http://chemistry.boisestate.edu/people/richardbanks/organic/nomenclature/acidnomenclature1.htm)
Muhlenberg – Nomenclature of Carboxylic Acid and Acid Derivatives (http://www.muhlenberg.edu/depts/chemistry/chem201woh/aciddern.html)
Jim Clark – Introducing Carboxylic Acid (http://www.chemguide.co.uk/organicprops/acids/background.html)
Latest posts by Krisna Dwi Wardhana (see all)



2 comments