Titrasi Asam Basa (netralisasi)
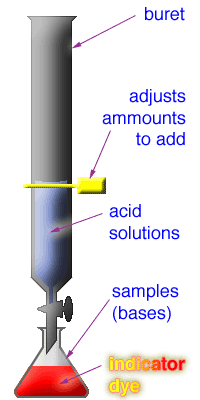 TITRASI ASAM BASA
TITRASI ASAM BASA
Prinsip Dasar
Titrasi netralisasi adalah titrasi yang didasarkan pada reaksi antara suatu asam dengan basa
H3O+ + OH– ⇔ 2 H2O
Dalam titrasi ini berlaku hubungan :
jumlah ekivalen asam (H3O+) sama dengan jumlah ekivalen basa (OH–).
Larutan baku yang digunakan pada titrasi netralisasi adalah asam kuat atau basa kuat, karena zat-zat tersebut bereaksi lebih sempurna dengan analit dibandingkan dengan jika dipakai asam atau basa yang lebih lemah. Larutan baku asam dapat dibuat dari HCl, H2SO4 atau HClO4, sedangkan larutan baku basa dibuat dari NaOH atau KOH. Larutan baku primer adalah larutan yang konsentrasinya dapat ditentukan dengan perhitungan langsung dari berat zat yang mempunyai kemurnian tinggi, stabil dan bobot ekivalen tinggi kemudian dilarutkan sampai volume tertentu. Sedangkan larutan baku sekunder, konsentrasinya harus ditentukan terlebih dahulu dengan pembakuan/standarisasi terhadap baku primer.
Contoh:
Baku primer : Na2CO3, Na2B4O7, Kalium Hidrogen Ptalat (KHP), H2C2O4
Baku sekunder : HCl, H2SO4, NaOH, KOH
Titrasi netralisasi dapat berlangsung antara asam kuat dengan basa kuat; asam/basa lemah dengan basa/asam kuat seperti:
NH4OH + H3O+ ⇔ NH4+ + 2H2O (basa lemah dengan asam kuat)
CH3COOH + OH– ⇔ CH3COO– + H2O (asam lemah dengan basa kuat)
CH3COO– + H3O+ ⇔ CH3COOH + H2O (garam dengan asam kuat)
NH4+ + OH– ⇔ NH3 + H2O (garam dengan asam kuat)
Kedua contoh terakhir di atas menggambarkan titrasi garam monofungsional. Garam-garam tersebut dalam air mengalami hidrolisis menghasilkan larutan yang bersifat asam atau basa. Apakah garam-garam ini dititrasi dengan asam atau basa bergantung pada nilai Ka dan Kb. Bila nilai Ka>Kb (larutan lebih bersifat asam), maka garam tersebut dapat dititrasi dengan basa, bila sebaliknya (Ka<Kb), garam tersebut dapat dititrasi dengan asam. Titik ekivalen dicapai pada pH larutan CH3COOH atau NH4OH.
Asam-asam poliprotik/polifungsional (H3PO4, H3AsO4) bila dititrasi dengan basa kuat dapat mempunyai titik ekivalen lebih dari satu.
H3PO4 + NaOH –> NaH2PO4 + H2O (Titik Ekivalen I)
NaH2PO4 + NaOH –> Na2HPO4 + H2O (Titik Ekivalen II)
Titik ekivalen pertama ditentukan oleh pH larutan NaH2PO4/NaH2AsO4 dan titik ekivalen kedua oleh pH larutan Na2HPO4/Na2HAsO4. Garam-garam tersebut karena dapat terhidrolisis menjadi asam dan basa maka untuk:
Titik Ekivalen pertama : [H3O+] = √K1K2
Titik Ekivalen kedua : [H3O+] = √K2K3
Untuk garam-garam amfoter seperti NaHCO3, NaH2PO4, Na2HPO4 sifat larutannya ditentukan oleh nilai Ka dan Kb. Besarnya nilai Ka dan Kb menentukan apakah garam-garam tersebut sebaiknya dititrasi dengan asam atau basa. Bila nilai Ka>Kb maka sebaiknya garam tersebut dititrasi dengan basa kuat atau sebaliknya dengan asam kuat.
Seperti halnya asam-asam polifungsional, titrasi garam-garam seperti Na2CO3 dan Na3PO4 mempunyai titik ekivalen lebih dari satu. Garam tersebut dalam larutan bersifat basa sehingga dapat dititrasi dengan asam. Contoh:
CO32– + H3O+ ⇔ HCO3– + H2O
HCO3– + H3O+ ⇔ H2CO3 + H2O
Titik ekivalen pertama ditentukan oleh pH larutan NaHCO3 dan titik ekivalen kedua oleh pH larutan H2CO3
Titik akhir titrasi dan pemilihan indikator
Titik akhir titrasi ditentukan dengan memilih indikator yang warnanya berubah sekitar titik ekivalen. Misalnya pada titrasi larutan garam Na2CO3 dengan larutan HCl, titik ekivalen pertama terjadi pada [H3O+] = √K1K2 nilai pH sekitar 8,35. Jadi indikator yang dapat digunakan adalah fenolftalein (8,1 – 10) yang berubah dari merah menjadi tidak berwarna. Pada titik ekivalen kedua, [H3O+] = √Ka1 nilai pH = 3,17; dan indikator yang sesuai adalah jingga metil. Dengan indikator ini perubahan warna yang diamati kurang tajam. Untuk memperbaiki pengamatan pada titik ekivalen ini, larutan dapat dididihkan terlebih dahulu, sehingga gas CO2 keluar dan sifat larutan ditentukan oleh garam NaCl yang tertinggal. Kelebihan asam dititrasi dengan larutan baku basa, dengan demikian dapat digunakan indikator metil jingga.
Pada pemilihan indikator harus diperhitungkan pula zat apa yang digunakan sebagai titran (yang diisikan dalam buret). Misalnya pada titrasi larutan HCl dengan larutan NaOH. Jika larutan HCl dipakai sebagai titran, larutan analit bersifat basa, maka indikator fenolftalein yang ditambahkan pada analit berwarna merah. Hilangnya warna merah indikator terjadi pada pH 8,1; sedangkan titik ekivalen titrasi terdapat pada pH 7,0. Jadi hilangnya warna merah terjadi sebelum titik ekivalen tercapai. Karena itu sebaiknya dipakai indikator dengan trayek perubahan warna pada sebelum atau sekitar pH 7,0.
Percobaan 1 silahkan lanjut ke halaman 2
- Latihan Soal OSN Biologi SMA 2026 - May 15, 2026
- Latihan Soal OSN Kimia SMA 2026 dan kunci jawabannya - May 14, 2026
- Portal dan Akun yang Digunakan untuk Verval PTK 2026 - May 14, 2026



6 comments