Laporan Praktikum Nitrasi Fenol
Tujuan
Menitrasi fenol melalui reaksi substitusi aromatik elektrofilik
Teori Dasar
Aromatik benzen menyajikan suatu kestabilan yang unik pada sistem pi dan benzena tidak menjalani kebanyakan reaksi yang khas bagi alkena. meskipun demikian, benzena tak inert. Pada kondisi tertentu, benzena mudah bereaksi substitusi aromatik elektrofilik. Reaksi substitusi aromatik elektrofilik adalah reaksi dimana suatu elektrofil disubstitusikan untuk satu atom hidrogen pada cincin aromatik. Reaksi terpenting di kelas ini adalah nitrasi aromatik. Halogenasi aromatik dan lain lain pada praktikum ini dilakukan nitrasi fenol melalui reaksi subdtitusi aromatik elektrofilik
Alat dan Bahan
- Kalsium nitrat tetrahidrat 1,5 gr
- asam asetat
- asam salisilat
Cara Kerja
- Kalsium nitrat dilarutkan dalam asam asetat hangat dan asam salisilat ditambahkan ke campuran tersebut
- Larutkan asam salisilat dan larutan akan menjadi merah tu. Kemudian campuran ke 10 mL air dingin
- Setelah 4 jam, kristal kuning yang dipisahkan dan dicuci telah bebas dari asam. Dicuci dengan air dingin
Pengamatan dan Pengolahan Data
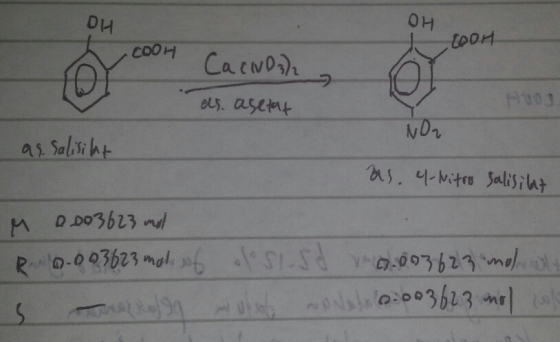
Campuran kalsium nitrat + asam asetat + asam salisilat –> merah
Didinginkan –> Terbentuk padatan
Disaring –> 1,55 gr – 0,48 gr = 1,07 gr
Massa produk:
mol x Mr = 0,003623 mol x 185 gr/mol = 0,66 gr
% Kesalahan Relatif = |(1,07 – 0,66) / 0,66 | x 100% = 62,12 %
Pembahasan
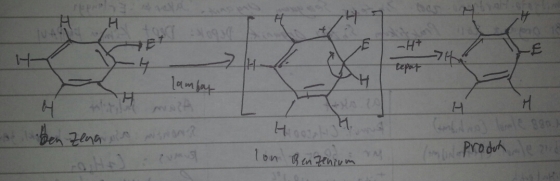
Pada percobaan kali ini akan dilakukan nitrasi fenol melalui reaksi substitusi aromatik elektrofilik. Nitrasi aromatik berupa 2 tahap reaksi pertama yaitu serangan elektrofilik. Elektrofiliknya ialah NO2+. Hasil dari serangan tersebut ialah ion benzenonium yang mengalami pelepasan H+ dengan cepat cepat dalam tahap kedua. Suatu elektrofil dapat menyerang elektron pi suatu cincin benzena untuk menghasilkan suatu macam karbokation yang terstabilkan oleh resonansi yang disebut disebut suatu ion benzenonium reaksinya :
Pada percobaan ini hal pertama yang dilakukan ialah menyiapkan reagen berupa asam salisilat, asam salisilat dan kalsium nitrat tetrahidrat. Asam salisilat berfungsi sebagai reagen utama yang akan dinitrasi kalsium nitrat tetrahidrat berfungsi sebagai sumber elektrofil yaitu NO2 dan asam asetat untuk pemberi suasana asam agar reaksi dapat berlangsung
Terbentuk larutan berwarna merah setelah semuanya larut dan didinginkan untuk pengkristalan dari produk selama 4 jam. Waktu ini dibutuhkan untuk waktu reaksinya agar maksimal. Reaksinya yaitu :
Pada percobaan ini didapatkan % kesalahan relatif sebesar 62,12 % dan yield yang melebihi 100% dan berarti telah jelas terjadi kesalahan dalam pelaksanaan praktikum. massa produk yang bereaksi kemungkinan ialah produk tak di inginkan atau reagen yang tidak ikut bereaksi, atau dari pengambilan reagen yang berlebih
Kesimpulan
- Massa asam 4-nitro-salisilat yang di dapat 1,07 gr
- % kesalahan relatif 62,12 %
- % Yield = 162,12%
- Substitusi aromatik elektrofilik adalah reaksi dimana suatu elektrofil disubstitusikan untuk satu atom hidrogen pada cincin aromatik
Daftar Pustaka
- Fessenden & Fessenden, 1982. Kimia Oragnik edisi 3. Jakarta : Erlangga
- Sastroamidjojo, Hardjono. 2009. Sintesis Senyawa Organik. Jakarta : Erlangga
- Tim KBI Organik. 2011. Praktikum Sintesis Organik. Depok: Departemen Kimia Fmipa UI
- Latihan Soal OSN Ilmu Komputer SMA 2026 - June 1, 2026
- Latihan Soal OSN Kebumian SMA 2026 - May 31, 2026
- Latihan Soal OSN Geografi SMA 2026 - May 30, 2026

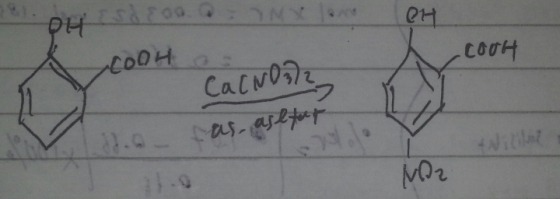

Leave a Reply