Laporan Praktikum Sintesis Dibenzalpropanon
Tujuan
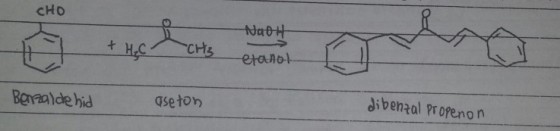
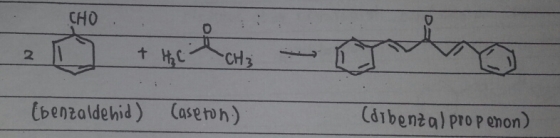
Mempelajari pembuatan dibenzalpropanon atau dibenzalaseton dari benzaldehid dan aseton atau propanon melalui kondensasi aldol
Teori Dasar
senyawa karbonil yang memiliki hidrogen yang terikat pada atom karbon α dapat mengalami reaksi kondensasi. Reaksi ini dilakukan dengan katalis basa yang berfungsi untuk membentuk ion karbon dengan mengikat atom Hα. Reaksi kondensasi ini banyak dijumpai, diantaranya reaksi pembuatan dibenzalpropanon. Reaksi antara suatu aldehid dengan suatu keton dengan adanya basa adalah suatu contoh reaksi kondensasi aldol(campuran aldehid-keton) yang disebut reaksi clasein-schmidt. Dibenzalpropanon dapat dibuat melalui reaksi kondensasi dari aseton dan dua ekuivalen benzaldehid. Gugus karbonil dari benzaldehid lebih reaktif dari gas karbonil aseton sehingga bereaksi cepat dengan anion asetat menghasilkan βHidroksi Keton. Senyawa hidroksi keton ini selanjutnya dengan mudah mengalami dehidrasi dengan katalis basa. Tergantung pada jumlah relatif pereaksi yang digunakan. Reaksi dapat menghasilkan mono atau benzaldehid
Alat dan Bahan
- Beaker gelas
- Bak es
- Stopwatch
- Corong
- Ring stand
- Kaca arloji
- Timbangan
- Gelas ukur
- Labu bulat
- Aseton
- benzaldehid
- NaOH 10%
- etanol
- Air
- ES
Cara Kerja
- Mencampurkan 3,8 mL larutan benzaldehid, 1 mL larutan aseton dan 15 mL larutan etanol lalu dikocok selama 2menit didalam labu bulat
- Tambahkan 30 mL larutan NaoH 10% dan dikocok selama 10 menit
- Pindahkan larutan tersebut ke beaker gelas yang ada di dalam bak es
- larutan disaring dan endapan yang didapat dicuci dengan aquades dan etanol
- Menimbang endapan atau kristal (dibenzalpropanon) yang mudah kering
Pengolahan Data
Massa kertas saring = 0,47 gr
Massa Total = 0,72 gr (kertas saring + endapan)
a. Secara percobaan
massa dibenzalpropanon = massa total – massa kertas saring = 0,72 gr – 0,47 gr = 0,25 gr
b. Secara Teoritis
m: 0,0368 mol 0,0143 mol
r : 0,0286 mol 0,0,143 mol 0,0143 mol
s : 0, 0082 mol – 0,0143 mol
mol benzaldehid = (3.9 gr)/(106,12 gr/mol) = 0,0368 mol
mol aseton = (o,83 gr)/(58,08 gr/mol) = 0,0143 mol
massa dibenzalpropanon = 0,0143 mol x 234,30 gr/mol = 3,35 gr
%Kesalahan Relatif = |(massa percobaan – massa teori) / Massa teori | x 100% = 92,5 %
%Yield = (massa percobaan / massa teori) x 100% = 7,46%
Pembahasan
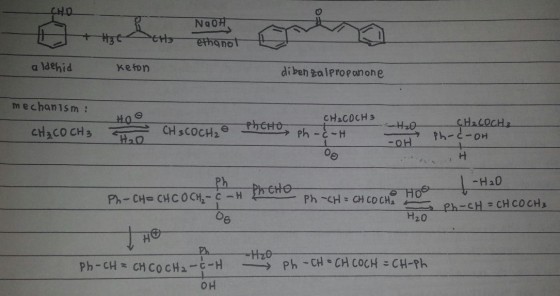
Senyawa aldehida yang mempunyai hidrogen α, jika berada dalam suasana basa akan mengalami adisi sesamanya menghasilkan produk yang dinamakan aldol, sedangkan reaksinya ialah reaksi aldol, reaksi aldol apabila diteruskan pada suhu yang relatif tinggi, akan berlanjut menjadi reaksi dehidrasi. Selanjutnya akan terbentuk produk akhir berupa senyawa α,β aldehid atau keton yang tidak jenuh. Reaksi aldol yang berlangsung sampai terjadi dehidrasi tersebut dinamakan reaksi aldol – kondensasi ( karena terjadi pelepasan molekul air , metanol, atau amonia). reaksi antara dua senyawa karbonil yang berbeda (salah satunya mempunyai α hidrogen) dalam suasana basa menghasilkan produk yang dikenal dengan nama kondensasi aldol campuran. sebagai contoh, reaksi antara benzaldehida (tidak mempunyai hidrogen α) dengan aseton dalam suasana basa akan menghasilkan produk dibenzalpropanon. Keton tidak mudah dioksidasi tetapi aldehid sangat mudah teroksisasi menjadi asam karboksilat. Hampir setiap reagensia yang mengoksidasi suatu alkohol juga mengoksidasi suatu aldehid.
Ikatan karbon hidrogen biasanya stabil, non polar dan pasti tidak bersifat asam. Tetapi dengan adanya suatu gugus karbonil terjadilah hidrogen α yang bersifat asam. jadi hidrogen yang berposisi α terhadap gugus karbonil bersifat asam. contohnya benzaldehid. Hal ini dikarenakan karbon alfa berdekatan dengan satu atau lebih atom karbon yang positif sebagian. karbon alfa itu juga ikut mengambil sebagian muatan positif ini (efek induksi), sehingga ikatan C-H menjadi dilemahkan dan yang lebih penting ialah stabilitas resonansi dari ion enolat, yakni anion yang terbentuk bila proton terlepas. dari struktur resonansi tampak bahwa muatan negatif diemban oleh oksigen karbonil maupun oleh karbon α. Delokalisasi muatan ini menstabilkan ion enolat dan mendorong pembentukannya.
pada praktikum ini dilakukan sintesis dibenzalpropanon dengan menggunakan katalis basa. langkah pertama pada percobaan ini ialah mencampurkan benzaldehid, aseton, NaOH 10%, aquades . Semua dicampurakan dalam labu bulatm kemudian kocok. Peran dar ibenzaldehid dan aseton ialah sebagai reaktan dari dibenzalpropanon. Pengocokkan dilakukan secara simultan agar proses pencampuran terjadi lebih cepat, peran NaOH 10% dalam reaksi ini sebagai katalis basa, dimana katais adalah suatu molekul yang dapat mempercepat reaksi, dan menurunkan energi aktivasi, tetapi tidak ikut bereaksi. kemudian campuran didinginkan. dalam bak yang berisi es. Hal ini berfungsi untuk mempercepat terbentuknya endapan atau proses rekristalisasi. setelah terbentuk, endapan dicuci menggunakan ethanol. ethanol dapat menarik air ang masih ada di dalam campuran dan juga mudah untuk menguap kembali.
Kondensasi aldol sangatlah penting dalam sintesis organik karena menghasilkan ikatan karbon karbon dengan baik. kondensasi aldol umumnya melibatkan adisi nukleofilik sebuah enolat keton ke sebuah aldehid membentuk β hidroksi keton atau sebuah aldol. sebuah unit struktural yang dijumpai pada molekul dalam obat obatan. Nama kondensasi aldol juga umumnya digunakan untuk merujuk reaksi aldol itu sendiri yang dikatalisasi oleh aldosanya. Jadi pada reaksi aldol ini sebenarnya bukanlah reaksi kondensasi karena dia tidak melibatkan pelesanan molekul yang kecil
Faktor kesalahan terjadi akibat ketidak telitian praktikan dalam mengukur volume reagen atau dikarenakan penyucian alat praktikum yang kurang bersih, dan salah pengambilan reagen menyebabkan proses rekristalisasi kurang sempurna
Kesimpulan
- Pembuatan dibenzalpropanon dilakukan dengan reaksi aldol kondensasi antara benzaldehid dengan aseton dalam suasana basa
- NaOH berfungsi katalis dalam dalam proses sintesis dibenzalpropanon
- Ethanol berfungsi sebagai penjembatani antara NaOH dengan reaktan
Daftar Pustaka
- Hart Crane Hart. 2003. Kimia Organik suatu kuliah singkat. jakarta
- Fessenden & Fessenden. 1984. Kimia Organik jilid 1. Jakarta. Erlangga
- Tim KBI Organik. 2008. Penuntun Praktikum SKO. Depok. FMIPA UI
- Latihan Soal OSN Kimia SMA 2026 dan kunci jawabannya - May 14, 2026
- Portal dan Akun yang Digunakan untuk Verval PTK 2026 - May 14, 2026
- Latihan Soal OSN Fisika SMA 2026 dan kunci jawaban - May 13, 2026

Leave a Reply