Rangkuman Klasifikasi Ligan Ligan (Bagian 1)
Senyawa koordinasi adalah senyawa yang mengandung satu atau lebih ion kompleks dengan sejumlah kecil molekul atau ion di seputar atom atau ion logam pusat, biasanya dari logam golongna transisi.(chang, 2005)
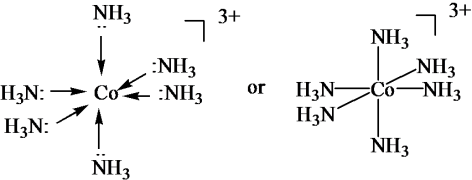
Ligan adalah molekul sederhana yang dalam senyawa kompleks bertindak sebagai donor pasangan elektron (basa Lewis). ligan akan memberikan pasangan elektronnya kepada atom pusat yang menyediakan orbital kosong. interaksi antara ligan dan atom pusat menghasilkan ikatan koordinasi. Pada gambar diatas, molekul NH3 yang bertindak sebagai ligan.
Klasifikasi Ligan
Ligan diklasifikasikan berdasarkan beberapa sifatnya. Yaitu:
- Berdasarkan sifat pasangan elektron yang mendonasi, ligand diklasifikasikan menjadi donor pas. elekron bebas, ikatan– π, ikatan-σ.

1.a Donor pasangan elektron bebas
Senyawa-senyawa yang memiliki pasangan elektron bebas pada kulit terluarnya dapat menjadi pendonor pasangan elektron bebas yang bertindak sebagai basa lewis
Pada gambar diatas telihat :NH3 sebagai contohnya, N yang masih memiliki pasangan elektron bebas dapat mendonorkannya pada atom pusat sehingga terbentuk ikatan koordinasi yang menjadi senyawa kompleks.
Ligand yang memberikan pasangan elektron sehinga membentuk ikatan σ M-L disebut sebagai σ donor.

Beberapa ligand pendonor pas-e bebas mungkin membentuk ikatan π M-L bonds. Disebut π donor, π acceptor. Ligand pendonor elektron pada logam membentuk ikatn- π disebut π donor
Misalnya pada 2 senyawa ini, sudut dari –O– membentuk 120 dan 180, berbeda dari air yang hanya 104,5 . hal ini disebabkan adanya π donor pada senyawa tersebut yang membuat sudut ikatannya membesar akibat tolakan yang lebih kecil karena pemakaian elektron elektron bebasnya untuk didonorkan sebagai π donor.
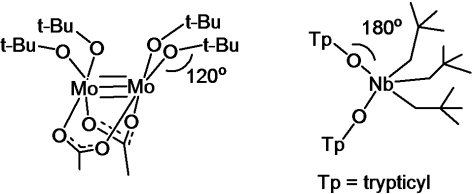
Beberapa ligan dapat bertindak sebagai phi donor atau pun sigma donor, dan juga sekaligus phi akseptor ataupun sigma akseptor. Beberapa diantaranya yaitu sebagai berikut :

1.b Ligand pendonor pasangan elektron – π bonding
Senyawa senyawa tersebut dapat menjadi donor pasangan elektron – π bonding pada atom logam.
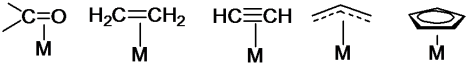
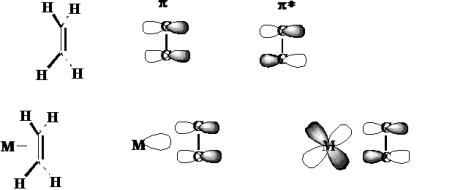
Ligan yang memiliki ikatan phi yang bisa melakukan donor pasangan elektron phi bonding. Pada Contoh, etilen memiliki yang memiliki orbital kosong disekelilingnya dapat menjadi phi akseptor. Namun yang bisa terjadi jika etilen anti-bonding karena akan cocok berinteraksi dengan atom logam.
Hapticity ligand:
ligand mungkin memiliki lebih dari satu cara untuk berikatan dengan atom pusat.
Hapticity sendiri digunakan untuk menggambarkan bagaimana atom-atom dari suatu ligan berkoordinasi dengan atom pusat. Pada penulisan nama, hapticity berupa huruf yunani “eta” η, diikuti dengan pangkat angka yang menunjukkan jumlah dari hapticity-nya.
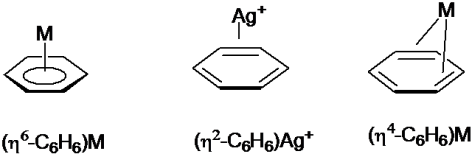
1.c Ligand pendonor pasangan elektron – σ
Gambar dibawah menunjukkan perbedaan posisi ikatan antara logam dan ligan yang menghasilkan ikatan sigma dan ikatan phi.

Yang membedakan terjadinya kedua macam ikatan seperti pada gambar diatas yaitu akibat perbedaan logamnya, atom logam yang memiliki Bilangan Oksidasi rendah, cenderung akan melakukan ikatan sigma, dan berlaku sebaliknya. Contohnya pada gambar dibawah.
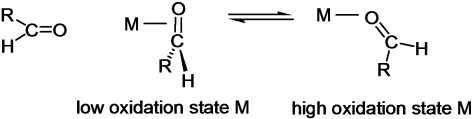
* Kebasaan relatif dari pasangan elektron:
elektron bebas > pasangan elektron p > pasangan elektron s
* Oleh karena itu kemampuan berikatan:
donor pas-e bebas > donor elektron p > donor elektron s.
- Latihan Soal OSN Ilmu Komputer SMA 2026 - June 1, 2026
- Latihan Soal OSN Kebumian SMA 2026 - May 31, 2026
- Latihan Soal OSN Geografi SMA 2026 - May 30, 2026




Leave a Reply