Soal Soal
elektrofil, inorganic chemistry, kimia anorganik, kompleks, LAJU REAKSI, LFSE, ligand, logam, mekanisme reaksi anorganik, nukleofil, outer sphere, reaksi assosiatif, reaksi dissosiatif, soal dan pembahasan mekanisme reaksi anorganik, soal kimia, soal kimio anorganik
Krisna Dwi Wardhana
0 Comments
Soal Latihan Dan Jawaban Mekanisme Reaksi Anorganik
Soal 1. Klasifikasikanlah molekul atau ion berikut ini, apakah nukleofi atau elektrofil, dan berikan alasannya ?
a. NH3 : Nukleofil
b. Cl : Nukleofil
c. Ag : elektrofil
d. S2- : Nukleofil
e. Al3+ :elektrofil
soal 2. Perhatikan reaksi berikut ini: Ni(CO)4 + L –> Ni(CO)3L + CO
Bila L adalah phospfane (PPh3) atau phosphit (PO32-) laju reaksinya tdak berbeda (tetap sama)
apakah reaksi tersebut dissosiatif atau assosiatif ?
Jawab: reaksi adalah dissosiatif
Soal 2. Berikan gambaran mengenai perbedaan mekanisme:
a) Dissosiatif(D)
b) Assosiatif (A)
c) Dissociative Interchange (Id)
d Associative interchange (Ia)
Gambarkan diagram profil energi untuk setiap mekanisme diatas dan ramalkanlah struktur dan intermediete setiap kasus
soal 3. senyawa kompleks cenderung mengalami reaksi pertukaran ligand dengan segera dan variasi laju yang sangat cepat, misalnya
[Fe(H2O)6]3+ + SCN- –> [Fe(H2O)5(SCN)]2+ +H2O
Reaksi ini sempurna pada saat larutan dicampurkan.
Kontras dengan reaksi berikut ini:
[Co(NH3)6]3+ + 6 H2O –> [Co(H2O)6]3+ + 6 NH4+
Walaupun dalam suasana asam, reaksi berlangsung sangat lambat (dalam waktu mingguan!) walaupun nilai AG < 0
Jelaskan mengapa ada perbedaan waktu yang sangat besar dalam kedua reaksi tersebut diatas.
(petunjuk : jelaskan masing masing kompleks dengan mempertimbangkan dengan konsep labilitas, inertness, stabilitas)
soal 4. Laju dan tetapan kesetimbangan reaksi, aquasi dan [Co(NH3)5X]2+ adalah:
[Co(NH3)5X]2+ + H2O –> [Co(NH3)5(H2O)]3+ X-
adalah
a. Plot data tersebut (log K vs log k) dan apa kesimpulan anda ?
b. Buat urutan kestabilan kompleks tersebut terhadap reaksi aquasi dan jelaskan alasan anda mengenai labilitas kompleks [Co(NH3)5X]2+
(cara menjawab lihat C.E. Housecroft & a.G sharpe,” inorganic chemistry, 3rd Ed, p 887 dan 891)
Soal 5. Reaksi antara [Pt(NH3)4]2+ dengan Cl- menghasilkan trans [Pt(NH3)2Cl2] dengan tanpa produk isomer-cis.
a. Tuliskan stoikiometri reaksinya
b. Jelaskan mengapa hanya produk-trans dan tidak ada produk isomer-cis
(cara menjawab lihat C.E. Housecroft & a.G sharpe, “Inorganic chemistry, 3rd Ed, p 885)
soal 6
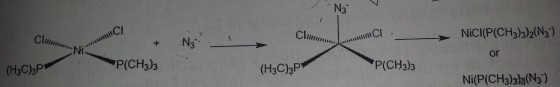
Reaksi substitusi ligand dari kompleks:
NiCl2(P(CH3)3)2 + N3- –> NiCl(P(CH3)3)2(N3) + Cl-
(i) Tentukan mekanisme substitusinya, assosiatif atau dissosiatif. Jelaskan dan berikan alasannya
JAWAB:
Mekanismenya adalah assosiatif. Karena senyawa tersebut adalah kompleks 16 electron maka dapat mengambil densitas elektron yang lebih (lebih banyak). Ligand Cl ukurannya kecil dan trimethyl phosphines tidak cukup besar untuk menghalangi ligand datang. JUGA, kompleks mempunyai bilangan koordinasi 4 sehingga tidak jenuh koordinasi.
(ii) Tentukan mekanisme reaksi yang terjadi !
Jawab :
(ii) Bila anda melakukan eksperimen menentukan kinetika reaksi tersebut. Bagaimana anda dapat melakukannya ?
JAWAB
Dengan eksperimen kinetika. Dengan cara merubah konsentrasi ligand datang dan mengobservasi laju reaksinya. Bila laju reaksi berubah seiring dengan perubahan konsentrasi ligand datang maka dapat diketahui bahwa mekanisme reaksi tersebut adalah mekanisme associative Bila tidak ada perubahan dengan perubahan konsentrasi ligand datang, maka mekanismenya adalah dissociative.
Soal 7. Untuk reaksi
[Co(NH3)5(H2O)]3+ + X- –> [Co(NH3)5X]2+ + H2O
Ternyata diperoleh persamaan laju :
Dan untuk X = Cl- nilai AV++ (volume aktivasi) adalah positif.
Jelaskanlah data tersebut
(lihat mekanisme Eigen Wilkins, dan CFSE oktahedral, d1 – d10)
NOTE: ΔV++ cenderung D atau Id
(cara menjawab lihat CE Housecroft a.G sharpe Inorganic chemistry, 3rd Ed, p 889-891)
Soal 7. Jawablah pertanyaan berikut ini:
(a) Reaksi Anasi
[Co(NH3)5(H2O)]2+ + Cl- –> [Co(NH3)5Cl]+ + H2O
Diperkirakan berlangsung melalui mekanisme Id.
Apa langkah elementer (elementary steps) yang terlibat dalam reaksi ini? Gunakan langkah ini untuk membedakan antara mekanisme reaksi ini dan mekanisme intimate reaksi ini
JAWAB
(a) Dalam mekanisme Id : seiring dengan mulai putusnya ikatan Co-OH2, Co mulai membentuk ikatan baru dengan Cl. Gugus masuk (datang) Cl harus berada dalam daerah ruang kompleks [Co(NH3)5(H2O)2+ pada saat ikatan Co-OH2 mulai putus. Jadi, sebelum terjadi substitusi, Cl harus masuk ke ‘outer sphere’ dari [Co(NH3)5(H2O)]2+
[Co(NH3)5(H2O)]2+ + Cl- –> {[Co(NH3)5(H2O)]Cl}+ + outer-sphere
Ligand OH2 dan Cl bertukaran dalam rds ( langkah penentu laju, rate determining step),
{[Co(NH3)5(H2O)]Cl}+ outer-sphere -(k)-> [Co(NH3)5Cl],H2O)]2+ outer-sphere
sebelum air secara sempurna meninggalkan outer sphere dari[Co(NH3)Cl]+ ,
{[Co(NH3)5(H2O)],Cl}+ outer-sphere –>(fast) [Co(NH3)5Cl]+ + H2O
Koleksi sekumpulan langkah elementer ini membentuk stoikiometri atau mekanisme reaksi
Langkah penentu laju, rds-The rate determining step, adalah langkah kedua dimana ligand bertukar tempat. Mekanisme intimate adalah penjelasan rinci/ details dari langkah ini.
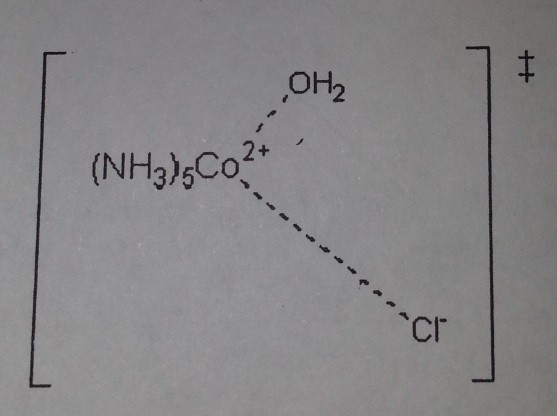
Untuk mekanisme Id keadaan transisi untuk langkah ini awal putusnya ikatan Co-OH2 dimulai pada saat Cl masih jauh :
(b) untuk kation logam transisi 3d berikut ini, laju pertukaran air berlangsung dengan urutan berikut ini:
Cr3+ < Fe3+ < Ni2+ < Co2+ < Mn2+ < Cr2+
Faktor apakah yang diperkirakan mengapa urutannya seperti diatas?
JAWAB:
(b) Dalam mekanisme D atau Id, putusnya ikatan membuat/ memberikan kontribusi dominan terhadap energi aktifasi Pembentukan intermediete Koordinat-5 atau kedaan transisi seperti pada gambar diatas membutuhkan hilangnya ikatan secara sempurna atau sebagian saja.
Jadi, lajunya lebih lambat untuk ion M 3+dibandingkan untuk ion M2+ karena ikatan dengan “lebih kuat. Dalam deret yang diberikan, pertukaran pada ion +3 lebih lambat dibandingkan ion +2.
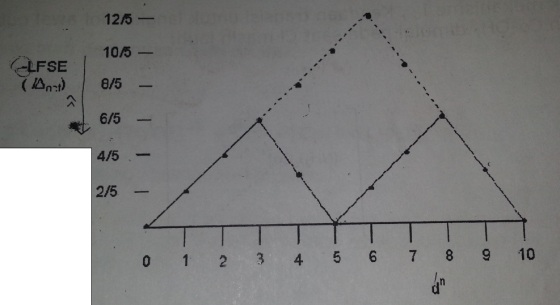
Untuk logam transisi, perubahan ligand-field stabilization energy (LFSE) memberikan sumbangan terhadap energi aktifasi. Untuk sistem octahedral, ini bervariasi dengan dn sesuai dengan kurva ‘double hump’:
Laju untuk Cr3+(d3) lebih lambat dibandingkan Fe3+ (d5) seiring dengan hilangnya (berkurangnya) LFSE untuk Cr3+ (d3) lebih besar bila simetri octahedral nya hilang
sama halnya, Ni2+ (d8) bertukar lebih lambat dari co2+ (d7) dan Mn2+ (d5). Yang paling labile adalah Cr2+ karena ground state sudah mirip (menyerupai) keadaan transisi karena adanya pemanjangan Jahn-Teler dari dalam kompleks d4
(c) Untuk Kation Logam, laju pertukaran air ternyata meningkat seiring dengan menurunnya gugus. Apa pendapat saudara mengenai hasil observasi ini.
JAWAB:
(c) Laju bertambah pada kelompok logam alkali (menurun kebawah tidak menunjukkan apakah mekanismenya associative atau dissociative, dan penjelasan berdasarkan pada salah satu atau kedua pathways adalah memungkinkan.
ukuran kation bertambah (menurun dari atas kebawah) dalam kelompoknya, sehingga pembentukan bingan koordinasi yang lebih tinggi dalam keadaan transisi assosiatif menjadi lebih mudah.
o Densitas muatan kation, semakin kebawah (dalam golongan yang sama) berkurang sehingga ikatan M – OH2 melemah dan pembentukan bilangan koordinasi yang lebih rendah (lebih kecil) dalam keadaan transisi dissociative juga menjadi lebih mudah.
LATIHAN
SL
Latest posts by Krisna Dwi Wardhana (see all)
- Latihan Soal OSN Ekonomi SMA 2026 - May 29, 2026
- Latihan Soal OSN Astronomi SMA 2026 - May 28, 2026
- Kumpulan Masalah Umum Verval PTK dan Solusinya (FAQ Lengkap) - May 27, 2026





Leave a Reply