Ringkasan Materi Konsep Mol

HITUNGAN KIMIA SEDERHANA
Contoh Soal : Hitunglah volume gas hidrogen (STP) yang terbentuk jika 5,4 gram Al (Ar = 27) dilarutkan dalam asam sulfat
- Menuliskan persamaan reaksi yang setara
Al(s) + H2SO4(aq) → Al2(SO4)3(aq) + H2(g) …. Belum setara
2Al(s) + 3H2SO4(aq) → Al2(SO4)3(aq) + 3H2(g) …. Sudah setara
- Menyatakan jumlah mol yang diketahui
Mol Al = gr Al/Ar Al = 5,4gr/27 = 0,2 mol
- Menentukan jumlah mol yang ditanya berdasarkan perbandingan koefisien reaksi
Mol H2 = Koefisien H2 / Koefisien Al = 3/2 x 0,2 mol = 0,3 mol
Menyesuaikan jawaban dengan pertanyaan
Volum H2 = 0,3 mol x 22,4 L/mol = 6,72 L
PEREAKSI PEMBATAS
Terjadi ketika jumlah pereaksi yang dicampurkan tidak dalam jumlah yang sebanding, sehingga akan ada pereaksi yang bersisa. Pereaksi yang habis disebut pereaksi pembatas.
Contoh Soal : Sebanyak 8 gram gas metana dibakar dengan 40 gram oksigen. Berapa gram CO2 yang terbentuk ? (H = 1; C = 12; O = 16)
- Setarakan reaksi yang terjadi (pembakaran metana) :
CH4 + 2O2(g) → CO2(g) + 2H2O(g) - Menyatakan jumlah mol yang diketahui. Pereaksi pembatas : CH4
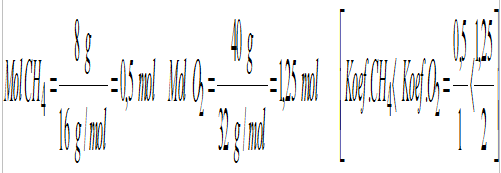
- Karena CH4 adalam pereaksi pembatas, maka :
mol CO2 = (Koefisien CO2 / Koefisien CH4) x mol CH4 = 1/1 x 0,5 mol = 0,5 mol
- Menyesuaikan jawaban dengan pertanyaan
Massa CO2 = mol CO2 x Mr CO2 = 0,5 mol x (12 + 32) gr/mol = 22 gram
Demikian ialah Ringkasan Materi Konsep Mol yang di sertai dengan soal dan pembahasan untuk perhitungan mol dan pereaksi pembatas
- Latihan Soal OSN Geografi SMA 2026 - May 30, 2026
- Latihan Soal OSN Ekonomi SMA 2026 - May 29, 2026
- Latihan Soal OSN Astronomi SMA 2026 - May 28, 2026



1 comment