Ringkasan Materi : Struktur Atom
A. Partikel penyusun Atom
Berdasarkan teori atom Dalton, atom merupakan partikel terkecil materi yang tidak dapat terbagi lagi. Teori atom ini dapat menjelaskan hukum kekekalan massa dan hukum perbandingan tetap, tetapi tidak dapat menjelaskan tentang sifat listrik materi dan daya gabung unsur-unsur.
| Partikel | Simbol | Muatan | Penemu |
| Proton | 1p1 | +1 | Goldstein (1886) |
| Neutron | 0n1 | 0 | James Chadwick (1932) |
| Elektron | -1e0 | -1 | J.J. Thomson (1897) |
| Inti atom | Rutherford (1910) | ||
| Kulit elektron | Niels Bohr (1914) |
Penemuan Elektron
Penemu elektron adalah J.J Thomson melalui percobaan sinar katode.
Muatan elektron ditemukan oleh Robert Milikan melalui percobaan tetesan halus minyak.
Sifat-sifat Sinar katode:
- merambat tegak lurus dari permukaan katode menuju anode
- merupakan radiasi partikel, terbukti dapat memutar kincir
- bermuatan listrik negatif sehingga dibelokkan ke kutub positif
- dapat memendarkan berbagai jenis zat, termasuk gelas
Penemuan Proton
Penemu proton adalah Eugene Goldstein melalui percobaan sinar katode yang telah dimodifikasi, yaitu memberi lubang (saluran) di tengah katode.
Sifat-sifat Sinar Anode (sinar terusan):
- merupakan radiasi partikel (dapat memutar kincir)
- dalam medan listrik/magnet dibelokkan ke kutub negatif, jadi merupakan radiasi bermuatan positif
- partikel sinar terusan tergantung pada jenis gas dalam tabung
Penemuan Neutron
Penemu neutron adalah James Chadwick melalui percobaan dengan menembaki atom Berilium dengan sinar alfa. Neutron tidak bermuatan.
Penemuan Inti Atom
Penemu inti atom adalah Ernest Rutherford bersama dua muridnya yaitu Hans Geiger dan Ernest Marsden dengan nama Eksperimen penghamburan sinar alpha.
Inti atom tersusun atas proton dan neutron. Proton dan neutron disebut nukleon.
B. Nomor Atom dan Nomor Massa
Nomor Atom (Z)
Nomor atom suatu unsur sama dengan jumlah proton. Untuk atom netral, jumlah proton = jumlah elektron
No. Atom = Jumlah proton = Jumlah elektron
Contoh : Atom Oksigen bernomor atom 8 sehingga memiliki 8 proton dan 8 elektron.
Nomor Massa (A)
Nomor massa adalah jumlah nukleon (proton dan neutron) yang terdapat dalam inti atom.
No. Massa = Jumlah proton + Jumlah neutron
Contoh : Atom natrium terdiri atas 11 proton dan 12 neutron, berarti nomor massa atom natrium = 11 + 12 = 23
Lambang Unsur (X)
Susunan suatu unsur netral dapat dinyatakan dengan lambang:
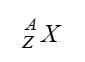
Dimana :
X = lambang unsur/notasi unsur
Z = nomor atom
= jumlah proton dalam inti (p)
= jumlah elektron yang mengelilingi inti
A= nomor massa
= jumlah proton + jumlah neutron (n)
n = neutron (n = A – Z)

C. Isotop, Isobar, dan Isoton
- Isotop
Isotop adalah atom-atom unsur yang mempunyai nomor atom sama (proton) tetapi nomor massanya berbeda.
Contoh :
Karbon alam terdiri atas 2 jenis isotop yaitu 6C12 dan 6C13
- Isobar
Isobar adalah atom-atom unsur yang berbeda (nomor atom berbeda) tetapi mempunyai nomor massa yang sama.
Contoh :
Isotop 6C14 adalah isobar dengan isotop 7N14
- Isoton
Isoton adalah atom-atom unsur yang berbeda (nomor atom berbeda) tetapi mempunyai jumlah neutron yang sama.
Contoh :
Isotop 6C13 dan isotop 7N14 adalah isoton (keduanya mempunyai 7 neutron).
D. Konfigurasi Elektron dan Elektron Valensi
Konfigurasi Elektron
Konfigurasi elektron menggambarkan penyebaran atau susunan elektron dalam atom. Pengisian elektron pada kulit-kulit atom memenuhi aturan-aturan tertentu, yaitu:
- Jumlah maksiumum elektron pada suatu kulit memenuhi rumus 2n2, dengan n = nomor kulit.
Contoh :
- Kulit K (n = 1) maksimum 2 . 12 = 2 elektron
- Kulit L ( n = 2) maksimum 2. 22 = 4 elektron
- Kulit M ( n = 3) maksimum 2 . 32 = 18 elektron
2. Jumlah maksimum elektron pada kulit terluar adalah 8
Contoh Soal:
- Konfigurasi elektron unsur Br (Z= 35), yaitu 2 8 18 7
- Konfigurasi elektron unsur Sn (Z= 50), yaitu 2 8 18 18 4
- Konfigurasi elektron unsur Fr (Z=835), yaitu 2 8 18 32 18 8 1
Elektron Valensi
Elektron valensi adalah elektron pada kulit terluar yang dapat digunakan untuk membentuk ikatan kimia. Susunan elektron valensi sangat menentukan sifat-sifat kimia suatu atom. Unsur-unsur yang memiliki struktur elektron valensi yang smaa memiliki sifat kimia yang sama.
Contoh :
11Na : K L M
2 8 18
Jumlah kulit = 3
Kulit terluar = M
Elektron valensi = 18
E. Perkembangan Teori Atom
- Model Atom Dalton
- Atom merupakan partikel terkecil suatu materi yang berbentuk bola.
- Atom tidak dapat diciptakan dan dimusnahkan
- Atom dari unsur yang sama mempunyai sifat yang sama, atom dari unsur yang berbeda mempunyai sifat yang berbeda pula
- Pada reaksi kimia terjadi penggabungan atau pemisahan atom-atom.

Kelemahan:
- Tidak dapat menjelaskan sifat listrik materi
- Tidak dapat menjelaskan daya gabung unsur-unsur. Misalnya mengapa satu atom oksigen dapat mengikat dua atom hidrogen membentuk air.
2. Model Atom J. J. Thomson
Setelah menemukan elektron, Thomson menggambarkan bahwa atom merupakan bola pejal bermuatan positif dan di dalamnya bertebaran elektron-elektron yang bermuatan negatif bagaikan kismis dalam roti kismis, secara keseluruhan atom bersifat netral.
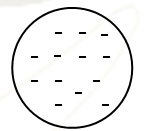
Kelemahan :
Tidak dapat menerangkan dinamika reaksi kimia yang terjadi antar atom.
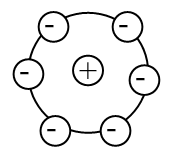
Model Atom Ernest Rutherford
Setelah menemukan inti atom, Rutherford mengemukakan model atom yang menyatakan bahwa atom terdiri atas inti atom yang bermuatan positif dan dikelilingi oleh elektron-elektron yang bermuatan negatif.



2 comments