LOGAM TITANIUM DAN APLIKASINYA SEBAGAI KATALIS
Pendahuluan
 Titanium adalah logam yang ringan dan kuat. Titanium sekuat baja dan dua kali lebih kuat seperti aluminium, tetapi 45% lebih ringan dari baja dan hanya 60% lebih berat dari aluminium. Titanium tidak mudah berkarat oleh air laut dan digunakan dalam baling-baling dan bagian lain dari kapal yang terkena air laut. Titanium dan alloy-nya digunakan dalam bagian pesawat terbang, rudal dan roket di mana kekuatan, berat yang rendah dan ketahanan terhadap suhu tinggi sangat penting. Karena titanium tidak bereaksi dalam tubuh manusia, digunakan untuk membuat pinggul buatan, pin untuk tulang serta untuk implan biologi lainnya. Sayangnya, tingginya harga titanium telah membatasi penggunaannya secara luas.
Titanium adalah logam yang ringan dan kuat. Titanium sekuat baja dan dua kali lebih kuat seperti aluminium, tetapi 45% lebih ringan dari baja dan hanya 60% lebih berat dari aluminium. Titanium tidak mudah berkarat oleh air laut dan digunakan dalam baling-baling dan bagian lain dari kapal yang terkena air laut. Titanium dan alloy-nya digunakan dalam bagian pesawat terbang, rudal dan roket di mana kekuatan, berat yang rendah dan ketahanan terhadap suhu tinggi sangat penting. Karena titanium tidak bereaksi dalam tubuh manusia, digunakan untuk membuat pinggul buatan, pin untuk tulang serta untuk implan biologi lainnya. Sayangnya, tingginya harga titanium telah membatasi penggunaannya secara luas.
Kata titanium berasal dari kata yunani Titan, sebuah makhluk mitologi Yunani “first sons of the Earth.Titanium ditemukan pada tahun 1791 oleh William Gregor, seorang pendeta Inggris. Titanium murni pertama kali diproduksi oleh Matthew A. Hunter, seorang metalurgi Amerika, pada tahun 1910. Titanium adalah elemen yang paling berlimpah kesembilan di kerak bumi dan terutama ditemukan dalam mineral rutil (TiO2), ilmenit (FeTiO3) dan sphene (CaTiSiO5). Titanium mempunyai komposisi sekitar 0,57% dari kerak bumi.
Fungsi Titanium
 Titanium dan alloy-nya banyak digunakan dalam berbagai bidang. Diantaranya :
Titanium dan alloy-nya banyak digunakan dalam berbagai bidang. Diantaranya :
- Karena kekuatannya, unsur ini digunakan untuk membuat peralatan perang (tank) dan untuk membuat pesawat ruang angkasa.
- TiO2, suatu pigmen putih permanen digunakan dalam cat, kertas, pasta gigi, dan plastik . TiO2 juga digunakan dalam semen, batu permata dalam, sebagai opacifier optik di kertas, dan sebagai penguatan dalam Tongkat pancing komposit grafit dan tongkat Bubuk TiO2 secara kimiawi inert, tidak memudar di bawah sinar matahari, dan sangat gelap: TiO2 ini memungkinkan untuk memberikan warna putih bersih dan cemerlang dengan coklat atau abu-abu bahan kimia yang membentuk mayoritas plastik rumah tangga .Di alam, senyawa ini. ditemukan dalam mineral anatase, brookite, dan rutil Cat dibuat dengan titanium dioksida. tidak baik dalam suhu yang parah, dan berdiri untuk lingkungan laut. Pure titanium dioksida memiliki indeks yang sangat tinggi bias dan dispersi optik lebih tinggi daripada berlian Selain menjadi pigmen yang sangat penting, titanium dioksida juga digunakan dalam tabir surya karena kemampuannya untuk melindungi kulit dengan sendirinya. Baru-baru ini, titanium oksida telah dimasukkan untuk digunakan di udara purifiers (sebagai. Filter coating), atau dalam film digunakan untuk melapisi jendela pada bangunan sehingga ketika titanium oksida menjadi terkena sinar UV (baik matahari atau buatan) dan kelembaban di udara, spesies redoks reaktif seperti radikal hidroksil yang dihasilkan sehingga mereka dapat memurnikan udara atau menjaga permukaan jendela bersih.
- Beberapa mesin pemindah panas (heat exchanger) dan bejana bertekanan tinggi serta pipa-pipa tahan korosi memakai bahan titanium.
- Bahan implan gigi, penyambung tulang, pengganti tulang tengkorak, struktur penahan katup jantung.
- Material pengganti untuk batang piston.
- Karena sifat Titanium yang kuat, ringan, dan tahan korosif air laut jadi untuk pembuatan pancingan.
Sifat – Sifat Titanium
Titanium adalah logam yang sangat ringan. Berat jenisnya hanya 4.5g/cm3, yang membuatnya hanya 4,5 kali lebih padat daripada air. Untuk membandingkan, dapat dilihat Timbal yang jauh lebih padat yang 11,3 kali lebih padat daripada air, dan aluminium yang lebih ringan, ringan sebesar 2,7 kali massa jenis air. Titanium memiliki kekuatan tertinggi untuk rasio kepadatan itu, dan hanya digunakan untuk area aplikasi bidang tertentu karena harganya yang tinggi.
| Fase | solid |
| Massa jenis(mendekati suhu kamar) | 4.506 g·cm−3 |
| Massa jeniscairan pada t.l. | 4.11 g·cm−3 |
| Titik lebur | 1941 K3034 °F 1668 °C, , |
| Titik didih | 5949 °F 3287 °C, 3560 K, |
| Kalor peleburan | 14.15 kJ·mol−1 |
| Kalor penguapan | 425 kJ·mol−1 |
| Kapasitas kalor | 25.060 J·mol−1·K−1 |
Karakteristik Ti dan Beberapa Logam Lain
| Ti | Fe | Ni | Al | |
| Melting Temperature (°C) | 1670 | 1538 | 1455 | 660 |
| Allotropic Transformation (°C) | β882 α | γ912α | – | – |
| Crystal Structure | bcc → hex | fcc → bcc | fcc | fcc |
| Room Temperature E (GPa) | 115 | 215 | 200 | 72 |
| Yield Stress Level (MPa) | 1000 | 1000 | 1000 | 500 |
| Density (g/cm3) | 4.5 | 7.9 | 8.9 | 2.7 |
| Comparative Corrosion Resistance | Very High | Low | Medium | High |
| Comparative Reactivity with Oxygen | Very High | Low | Low | High |
| Comparative Price of Metal | Very High | Low | High | Medium |
Struktur Logam Titanium
Titanium murni menunjukkan transformasi fase allotropic pada 882°C, berubah dari struktur kristal BCC (fase β) pada suhu yang lebih tinggi untuk struktur-padat kristal heksagonal (α fase) pada temperatur yang lebih rendah.

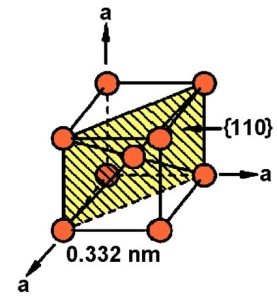
Unit sel fasa α Unit sel fasa β
Temperatur transformasi sangat dipengaruhi oleh unsur-unsur interstisial dan substitusi pada cristal dan oleh karena itu suhu tergantung pada kemurnian logam model kristal titanium membantu memprediksi bagaimana titanium akan melakukan deformasi peregangan atau lainnya karena deformasi akan cenderung terjadi di sepanjang bidang kristal yang menyelaraskan dan mengarahkan arah bidang terlemah dalam materi.
Aplikasi Logam Titanium sebagai Katalis
Pembuatan botol PET (Polietilentereftalat)
Dalam botol PET hot-fill dengan menggunakan katalis titanium lebih tahan terhadap penyusutan massa dibandingkan dengan botol PET dengan menggunakan katalis antimoni. Penggunaan katalis titanium juga memberikan warna pada botol PET menjadi lebih jernih karena adsorpsi cahaya yang diberikan oileh katalis titainum lebih baik dibandingkan dengan menggunakan katalis antimoni.
Katalis pada Sintesis Vinil Homopolimerisasi Norbornene
Katalis yang mengandung logam titanium, zirkonium, kobalt, kromium, nikel, dan paladium biasa digunakan pada proses homopolimerisasi vinil dari norbornen dan olefin siklik terterik secara 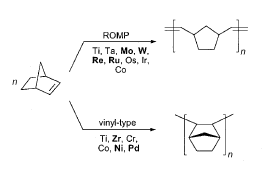 umum. Berdasarkan komposisi logamnya, katalis untuk polimerisasi vinil dapat dibagi menjadi tiga golongan: (a) logam transisi awal, terutama katalis metallocene zirkonium; logam transisi akhir seperti palladium (II) dan nikel (II) dan (c) logam transisi yang jarang digunakan seperti kromium dan kobalt.
umum. Berdasarkan komposisi logamnya, katalis untuk polimerisasi vinil dapat dibagi menjadi tiga golongan: (a) logam transisi awal, terutama katalis metallocene zirkonium; logam transisi akhir seperti palladium (II) dan nikel (II) dan (c) logam transisi yang jarang digunakan seperti kromium dan kobalt.
Katalis metallocene yang terdiri dari metallocene periode 4 (terutama zirkonium) dan metilaluminoksan (MAO). Tipe katalis ini dapat mempermudah proses polimerisasi alkena siklik tanpa pembukaan cincin.
Sintesis bis(tert-butyl)cyclopentadienyl derivatives
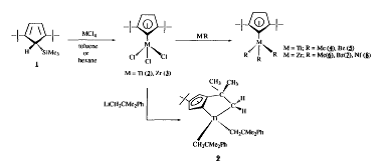
Metode yang umum digunakan untuk membuat kompleks monocyclopentadienyl adalah dengan mereaksikan Si (1,3-tBu2-CsH3) ME3 dengan MC14 (M = Ti, Zr) dalam toluena atau heksana pada suhu kamar, yang dapat meng isolasi derivat trikloro pada logam Ti dan Zr menjadi mikrokristalin padat.
Katalis Ziegler Natta
Katalis Ziegler-Natta, yang dinamai dari penemunya Karl Ziegler dan Giulio Natta, adalah katalis yang digunakan dalam sintesis polimer dari 1-alkena (α-olefin). Katalis Ziegler-Natta dibagi ke dalam dua kelas berdasarkan sifat kelarutannya , yaitu :
Katalis heterogen
Tipe katalis ini biasanya berasal dari logam titanium yang digunakan dalam reaksi polimerisasi dalam kombinasi dengan kokatalis, senyawa organoaluminum seperti triethylaluminium, Al(C2H5)3. Kelas katalis ini biasanya mendominasi industri.
Kelas katalis Ziegler-Natta heterogen yang paling dominan biasanya berbasis logam Ti (beberapa berbasis logam V). Kelas ini secara umum dapat dibagi menjadi dua sub-kelas, (a) katalis yang cocok untuk homopolimerisasi etilen atau alkena primer lainnya menjadi LLDPE (Linear Low Density Polyethylene), (b) katalis yang cocok untuk sintesis isotaktik 1-alkena.

Katalis homogen
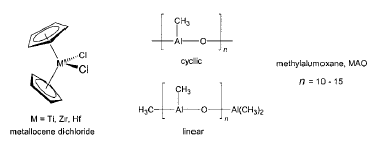
Tipe katalis ini biasanya mengandung kompleks Ti, Zr, atau Hf. Katalis ini biasanya digunakan dalam kombinasi dengan kokatalis organoaluminum yang berbeda yaitu methylaluminoxane (atau methylalumoxane, MAO). Katalis ini secara konvensional termasuk senyawa metallocenes tetapi jugaberbasis ligan multidentat oksigen dan nitrogen.
Katalis Ziegler-Natta yang homogen dapat larut dalam media reaksi atau pelarut. Tipe ini biasanya merupakan turunan dari metallocene tetapi struktur dari katalis aktifnya saat ini sangat beragam. Suatu katalis metallocene ideal memiliki komposisi Cp2MCl2, dimana Cp adalah siklopentadienil, Cl adalah klorida, dan M adalah atom logam pusat (M = Ti, Zr, Hf) seperti titanocene diklorida.
Ligan siklopentadienil juga dapat digantikan dengan ligan organik lainnya tetapi masih turunan siklopentadienil. Pada beberapa kompleks, kedua ligan siklopentadienil juga dapat dihubungkan dengan jembatan seperti –CH2-CH2– atau >SiPh2. Katalis metallocene dapat menghasilkan baik polimer isotaktik maupun sindiotaktik dari propilen dan 1-alkena lainnya.
Selain katalis metallocene, katalis Ziegler-Natta homogen lainnya termasuk ke dalam kelas katalis non-metallocene. Tipe katalis ini menggunakan beragam kompleks logam, bervariasi dari skandium hingga logam lantanida dan aktinida, juga variasi ligan yang mengandung oksigen, nitrogen, fosfor, dan sulfur. Kompleks diaktivasi menggunakan MAO seperti pada katalis metallocene.Kebanyakan katalis Ziegler-Natta dan semua kokatalis alkilaluminium tidak stabil di udara, sehingga selalu dipreparasi pada atmosfer inert.
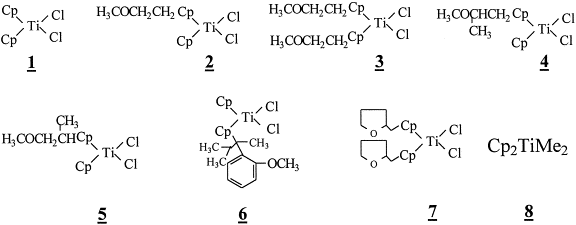
Mekanisme Polimerisasi Katalis Ziegler-Natta
Struktur dari pusat aktif katalis Ziegler-Natta yang pertama kali dapat dijelaskan adalah katalis metallocene. Kompleks metallocene Cp2MCl2 bereaksi dengan MAO dan bertransformasi menjadi ion metallocenium Cp2M+-CH3.
LnTi–CH2−CHR–Polymer + CH2=CHR → LnTi–CH2-CHR–CH2−CHR–Polymer
- Latihan Soal OSN Ekonomi SMA 2026 - May 29, 2026
- Latihan Soal OSN Astronomi SMA 2026 - May 28, 2026
- Kumpulan Masalah Umum Verval PTK dan Solusinya (FAQ Lengkap) - May 27, 2026



Leave a Reply