Teori Kimia
Teori Atom berkembang seiring dengan perkembangan ilmu pengetahuan. Sebelum Niels Bohr, banyak ilmuwan yang telah mengadakan percobaan dan menganalisis hasil percobaan tersebut serta membuat teori atom. Ilmuwan sebelum model atom Niels Bohr adalah John Dalton, J.J. Thomson, dan Ernest Rutherford.

John Dalton pada tahun 1805 mengemukakan teori atom berdasarkan hukum kekekalan massa dan perbandingan tetap sebagai berikut :
a. Semua materi tersusun dari partikel terkecil yang tidak dapat diciptakan dan dimusnahkan.
b. Atom-atom unsur sejenis adalah sama dalam segala hal, tetapi atom-atom unsur tidak sejenis berbeda dengan atom-atom lain.
c. Adanya ikatan antara senyawa yang terbentuk.
d. Atom-atom membentuk sebuah molekul dengan angka perbandingan bilangan bulat sederhana.

J.J. Thomson pada tahun 1897 menemukan elektron melalui percobaan dengan tabung sinar katode dan mengemukakan teori atom sebagai berikut :
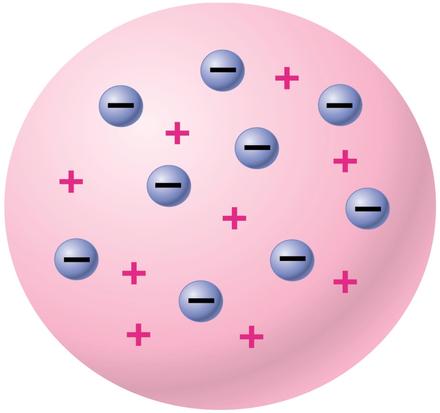
a. Atom merupakan bola yang bermuatan positif dan pada tempat tertentu elektron bermuatan negatif tersebar bagaikan kismis pada roti kismis.
b. Secara keseleruhan atom bersifat netral yaitu jumlah muatan positif sama dengan jumlah muatan negatif.

Ernest Rutherford pada tahun 1909 melakukan eksperimen bersama Hans Geiger dan Ernest Marsden dengan cara menembaki lempengan logam tipis dengan partikel sinar alfa berenergi tinggi sehingga Rutherford menemukan inti atom yang bermuatan positif dan massa atom terpusat di inti kemudian membuat model atom sebagai berikut :
a. Atom terdiri dari inti atom yang bermuatan positif dan elektron yang bermuatan negatif yang mengelilingi inti atom.
b. Atom bersifat netral.
c. Ukuran atom 10-8 cm dan inti atom 10-13 cm.
Teori atom ini memiliki kekurangan karena belum dapat menjelaskan bagaimana elektron- elektron tersusun di sekeliling inti atom tidak pernah jatuh ke inti.
Menurut fisika klasik, gerakan elektron mengitari inti disertai dengan kehilangan sejumlah energi, di mana energi kinetik berkurang secara terus-menerus sehingga lintasannya membentuk spiral dan akhirnya jatuh ke inti atom.

Niels Bohr pada tahun 1913 kemudian dapat menjelaskan teori Rutherford dengan spektrum unsur melalui teori Max Planck, sehingga Niels Bohr membuat model atom sebagai berikut :
a. Elektron dalam atom bergerak mengelilingi inti atom dengan tingkatan energi tertentu. Bilangan kuantum utama (n) makin besar harganya, maka kulittersebut makin jauh dari inti atom dan makin besar pula energi elektron pada kulit tersebut.
b. Elektron dengan jumlah energi tertentu akan tetap ada pada tingkat energitertentu.
c. Elektron dapat pindah dari tingkat yang satu ke tingkat yang lain dengan disertai pemancaran atau penyerapan sejumlah energi. Penyerapan energi terjadi pada peristiwa perpindahan elektron ke kulit lebih luar dan pelepasan energi terjadi pada peristiwa perpindahan elektron ke kulit lebih dalam.
Berikut ini adalah model-model atom mereka :
John Dalton :

J.J. Thomson :
Ernest Rutherford :
Niels Bohr :

- Latihan Soal OSN Kebumian SMA 2026 - May 31, 2026
- Latihan Soal OSN Geografi SMA 2026 - May 30, 2026
- Latihan Soal OSN Ekonomi SMA 2026 - May 29, 2026



Leave a Reply