SPEKTROSKOPI RESONANSI MAGNETIK INTI (NMR)
A. TEORI DASAR
Spektroskopi Resonansi Magnetik Inti (Nuclear Magnetic Resonance/NMR) adalah salah satu cabang dari spektroskopi absorbsi yang menggunakan radiasi frekuensi gelombang radio untuk menginduksi terjadinya transisi antara dua tingkat energi spin suatu inti yang mempunyai momen magnetik inti bukan nol.
1. Sifat Magnetik Inti dan Resonansi
Suatu inti dengan jumlah proton ganjil mempunyai muatan dan spin, sehingga mempunyai momen magnetik. Dalam sekumpulan atom, orientasi spinnya dalam ruang berada dalam keadaan acak. Namun demikian, jika diletakkan dalam medan magnet momen magnet tersebut akan terorientasi umpamanya inti hidrogen mempunya dua orientasi yang mungkin, yaitu satu spin searah dan yang lainnya berlawanan arah dengan medan magnet luar. Kedua orientasi tersebut mempunyai perbedaan energi (E) yang sangat kecil, dan dapat digambarkan seperti Gambar 1.

Gambar: 1. Orientasi spin inti hidrogen.
Jika atom-atom diletakkan dalam suatu medan magnet, dapat terjadi transisi antara kedua tingkat energi tersebut diatas, dengan jalan penyerapan energi terkuantum hv. Perbedaan energi kedua tingkat tersebut sangat kecil (sesuai dengan frekuensi gelombang radio). Hidrogen adalah atom yang hanya
mempunyai dua tingkat kuantum terinduksi oleh magnet, akan tetapi atom-atom dengan spin nuklir yang mempunyai banyak tingkat energi.
Inti suatu atom mempunyai momentum sudut intrinsik (dengan momen magnetnya yang sesuai), yang harganya merupakan kelipatan bilangan bulat atau tengahan dari h/2π, dan dinyatakan sebagai I(h/2π), I disebut bilangan kuantum spin nuklir. Momen magnet (μ) dihasilkan oleh perputaran atau rotasi muatan listrik pada inti. Bilangan kuantum spin dan momen magnet erat kaitannya dengan nomor massa dan nomor atom seperti terlihat pada Tabel 1. Inti dengan I = 0, seperti C12, O16 tidak mempunyai transisi NMR. Secara umum hanya molekul yang mempunyai spin inti ½ memberikan resolusi yang tinggi pada spektrum NMR. Inti dengan bilangan kuantum 1 atau lebih besar akan memberikan spektrum yang melebar disebabkan oleh momen kuadrupol listriknya.
Tabel 1. Bilangan kuantum spin inti (I), momen magnet (μ) dan momen kuadrupol (eQ).
Nomor massa | Nomor atom | I | μ | eQ | Contoh |
genap ganjil genap | genap genap atau ganjil ganjil | 0 ½ 1 | 0 ± ½ ± 1,0 | 0 0 0 | C12, O16, S32,S34 H1, C13, N15, P31 H2, N14 |
Inti dengan I = ½, yang paling penting dan kelimpahan isotopnya tinggi, adalah H1, F19, P31. Atom-atom tersebut dapat dipelajari dengan NMR. C13 mempunyai spin = ½ tetapi sensitifitasnya terbatas dan kelimpahan isotop alamiahnya hanya 1%.
Perbedaan energi antara kedua keadaan kuantum bergantung pada kekuatan medan magnet pada inti, sehingga :
= frekuensi radiasi
Ho = kuat medan magnet
= konstanta, perbandingan magnetogerik.
Dalam medan magnet Ho = 14,092 gauss, resonansi proton terjadi pada 60 MHz.
Spektrum NMR biasanya tajam oleh karena inti atomnya terisolasi, tabrakan antara atom-atom hanya mempengaruhi elektron luar, resolusi tinggi dihasilkan oleh sampel cair (termasuk larutan).Gas pada umumnya mempunyai inti terlalu sedikit untuk menghasilkan signal yang dapat diamati, dan inti pada sampel padat terlalu kuat dipengaruhi oleh medan kristalnya sehingga menimbulkan signal yang melebar.
2. Pergeseran kimia
Persamaan =
Ho/2π menunjukkan bahwa semua proton mengalami resonansi pada medan magnet yang sama (pada frekuensi tertentu). Jika demikian halnya, maka teknik ini tidak banyak gunanya untuk penentuan struktur. Pada instrumen resolusi tinggi, dapat diperoleh pemisahan puncak untuk masing-masing proton. Hal ini tidak bertentangan dengan pernyataan di atas, sebab Ho pada pernyataan tersebut adalah medan magnet pada inti, bukan medan magnet luar yang digunakan. Elektron dalam atom atau molekul bertindak sebagai tameng dan dapat sedikit mengubah medan magnet luar. Proses penamengan ini berbeda-beda untuk setiap jenis proton yang berbeda, dan bergantung pada lingkungan inti pada molekulnya. Dengan demikian proton pada gugus aldehida CHO akan mengalami resonansi pada medan magnet uyang berbeda dibandingkan dengan proton pada gugus CH3.
Pemisahan frekuensi resonansi suatu inti dari frekuensi resonansi suatu standar [biasanya TMS, (Tetra Metil Silan) Si(CH3)4] disebut pergeseran kimia, dan dinyatakan sebagai berikut :
merupakan tetapan yang tidak berdimensi dengan satuan ppm.
Jika kerapatan elektron disekitar proton berkurang karena adanya gugus yang elektronegatif (gugus yang magnetik), maka medan magnet terinduknya, yang berlawanan dengan medan magnet luar yang digunakan, akan berkurang kekuatannya. Dengan demikian proton akan beresonansi dengan oscilator RF pada medan magnet luar yang lebih rendah (H). Resonansi pada H yang lebih rendah ini disebut pergeseran kimia ke medan bawah ( down field ), dan yang lawannya disebut pergeseran ke medan atas. Pada gambar 2 dapat dibaca harga pergeseran kimia beberapa gugus fungsional organik yang penting.
3. Pemecahan Spin-spin (Spiltting), Konstanta Kopling dan Integrasi.
Posisi resonansi suatu proton dapat dipengaruhi oleh spin proton-proton yang ada di sebelahnya. Juga suatu proton dapat membuat suatu perubahan kecil dalam penamengan proton tetangganya melalui ikatan elektronik, maka akan terjadi pemecahan spin-spin atau pembentukan pasangan spin (spin coupling). Meskipun proton A dan proton B yang terikat pada dua karbon yang berdekatan (gambar 3) letaknya terlalu berjauhan untuk dapat saling mempengaruhi medan magnetnya melalui ruang, namun proton A dapat mempolarisasikan awan elektron di sekitarnya dan polarisasi ini dapat ditransmisikan melalui sistem ikatan ke proton B.
Melalui mekanisme ini , medan efektif proton B akan diperkuat atau diperlemah oleh medan magnet lokal A bergantung apakah medan A searah atau berlawanan arah dengan medan Ho (proton A terletak pada keadaan energi spin tinggi atau rendah). Dengan demikian garis resonansi akan bergeser sedikit kekiri atau kekanan dan pada spektrum dapat diamati garis B pecah menjadi dua (doublet). Oleh karena keboleh jadian proton A berada pada masing-masing tingkat energi spin sama, maka intensitas kedua garis akan sama. Demikian juga garis A dapat dipengaruhi oleh proton B. Jarak antara garis (puncak) dalam doublet tersebut disebut konstanta pembentukan pasangan J (coupling constant) lihat gambar-3.

Gambar 3. Pemecahan spin-spin dan konstanta kopling.
a. Pemecahan spin HA akibat pengaruh HB
b. Pemecahan spin HB akibat pengaruh HA
c. Puncak (spektrum) yang timbul akibat pengaruh 1 proton tetangga.
Pengaruh proton tetangga yang lebih dari satu, terhadap spektrum yang dihasilkan dapat diterangkan sebagai berikut. Sebagai contoh ambillah senyawa Etil klorida.
CH3 – CH2 – Cl ada 3 proton A yang ekivalen
A B ada 2 proton B yang ekivalen
Kombinasi orientasi spin kedua proton B dalam medan Ho adalah seperti berikut : (lihat gambar-4a)

Gambar 4a. Orientasi spin dari 2 proton yang ekivalen.
Jadi proton A dalam sampel dipengaruhi oleh 3 medan magnet B yang berbeda. Akibatnya akan terpecah menjadi tiga (triplet) dengan perbandingan luas puncak= 1 : 2 : 1
Bagai manakah orientasi spin 3 proton A yang ekivalen ? Hal ini dapat dilihat pada gambar 4b.
1
3
3
1
a1 a2 a3
Ho
Gambar 4b. Orientasi spin 3 proton yang ekivalen.
Jadi proton B akan dipengaruhi 4 medan magnet A yang berbeda, akibatnya akan terpecah menjadi empat (kuartet) dengan perbandingan luas = 1 : 3 : 3 : 1
Untuk pemecahan order pertama, secara umum suatu puncak akan pecah menjadi ( n+1 ) pucak karena pengaruh dari n proton tetangganya (yaitu H yang terikat pada atom-atom C disebelahnya) yang ekivalen. Perbandingan luas puncaknya (intensitasnya) dapat dinyatakan sebagai koefisien dari ( a+b )n atau seperti segitiga Pascal.


Gambar 4c. Segitiga Pascal.
Intensitas relatif untuk multiplet order pertama. n = Jumlah kopling inti ekivalen dengan spin ½ (misalkan proton). Integrasi dari luas puncak yang dihasilkan akan memberikan perbandingan bulat yang merupakan perbandingan jumlah proton yang terdapat pada puncak tersebut. Sebagai contoh adalah spektrum etilklorida ( gambar 5 ). Perbandingan tinggi integrasi puncak yang muncul pada ppm sekitar 3,5 dengan 1,5 adalah sebagai bilangan 2 : 3. Hal tersebut menunjukkan bahwa pada ppm 3,5 terdapat 2 proton (CH2) atau kelipatan dari 2 sedangkan pada ppm 1,5 terdapat 3 proton ( CH3 ) atau kelipatan dari 3 proton.
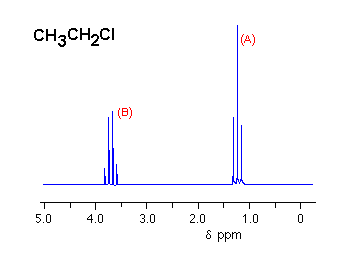
Gambar : 5, Spektrum etil klorida.
Aturan kopling order pertama berlaku selama frekuensi pemisahan ( A ) dari dua jenis proton ( A dan B) jauh lebih besar dari konstanta koplingnya atau δ / J >> 1.
Contoh lain dari pemecahan spin-spin adalah spektrum asetaldehida. Analisa senyawa tersebut dengan alat beresolusi rendah akan menghasilkan spektrum degan dua puncak, dimana luas puncak relatifnya merupakan perbandingan bilangan 3 : 1, sesuai dengan jumlah protonnya. Analisa dengan beresolusi tinggi memberikan spektrum yang berbeda. Puncak CH3 akan terpecah menjadi doublet dan proton CHO menghasilkan struktur kuadruplet. Struktur halus ini timbul karena kopling spin. Gugus metil terpecah menjadi doublet karena interaksi proton tersebut dengan dua keadaan spin dari proton gugus aldehida ( spin tinggi dan spin rendah ). Dalam hal lain, gugus aldehida terpecahkan menjadi kuanter akibat interaksi dengan proton gugus CH3.
Besarnya pecahan bergantung pada beberapa faktor. Jika dua proton yang berbeda secara magnetik, berada pada atom karbon yang sama, besarnya pemecahan (konstanta kopling) adalah antara 12 – 15 Hz dan terbentuk dua puncak doublet. Kedua atom hidrogen mempunyai lingkungan kimia yang berbeda dan frekuensi resonansinya terpisah sebesar pergeseran kimianya. Masing-masing dari kedua puncak tersebut terpecah oleh kopling spin dengan proton yang lainya.
Faktor yang mempengaruhi besarnya interaksi adalah :
1. Jarak antara proton.
2. Jenis ukuran atom antar proton.
3. Keadaan geometri.
Pemecahan tidak teramati untuk proton yang identik, dan besarnya “dalam Herz” tidak dipengaruhi oleh medan magnet yang digunakan.
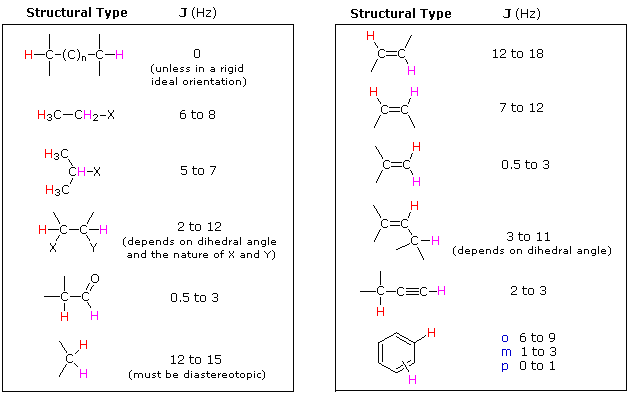
Gambar: 6. Beberapa contoh konstanta kopling.
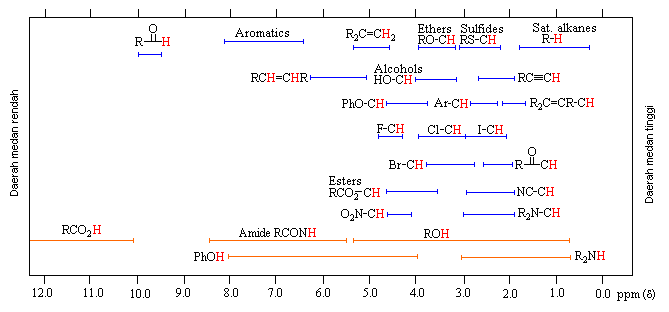
Gambar: 7. Pergeseran kimia proton pada bermacam gugus fungsi. Sampel diukur dengan pelarut CDCl3 dan dibandingkan dengan TMS pada = 0.
4. Peralatan.
Pada pokoknya spektrometer NMR terdiri atas 6 unit dasar, lihat Gambar-7
Magnet : magnet biasa atau elektromagnet yang mampu menghasilkan medan magnet kuat, setabil dan homogen untuk memisahkan tingkat energi inti.
Kumparan transmiter : untuk menghasilkan energi radiasi RF. Kumparan ini letaknya tegak lurus pada kumpulan penyapu (sweep coils).
“Sweep generator” : untuk menyapu medan magnet melalui daerah resonansi untuk menghasilkan spektrum.
Kumparan penerima : mengelilingi tempat sampel untuk merangkaikan sampel dengan penerima RF.
Detektor : untuk memproses signal-signal NMR.
Rekorder : untuk menggambar spektrum, baik mode absorbsi maupun integrasi.

Gambar : 8. Diagram skematik spektrometer NMR.
Tempat sampel, lihat gambar : 8, terletak pada madan magnet elektromagnet dengan medan RF yang tegak lurus terhadap medan magnet. Medan magnet dari kumparan sweep generator disapukan secara perlahan (menarik) ke daerah resonansi. Pada resonansi terjadi suatu perubahan pada dipol magnetik inti suatu voltase akan terinduksi ke kumparan penerima, yang lalu diperkuat, dideteksi dan dicatat. Spektrum yang dihasilkan merupakan gambaran antara energi transisi resonansi terhadap intensitas.
Sampel di letakkan pada suatu tabung gelas yang berdinding tipis dengan diameter luar 5 mm. Turbin tiupan udara akan memutar sampel dengan kecepatan beberapa ratus putaran tiap menit (rpm) untuk menjaga kehomogenan medan magnet yang mengenainya. Pada spektrum terdapat juga puncak-puncak tambahan yang dihasilkan oleh perputaran sampel, sebab pada frekuensi (kecepatan) putaran ini puncak-puncak resonansi mengalami sedikit perubahan.
5. Beberapa Penggunaan Spektrometer NMR.
Beberapa pemakaian umum dari studi penggunaan NMR meliputi :
Analisa Kuantatif, sebagai contoh penentuan campuran benzaldehida, etanol dan toluen.
Isomerisasi sis – trans.
Efek ikatan hidrogen pada pergeseran kimia.
Efek substitusi halogen pada hidrokarbon.
Penentuan struktur molekul.
Pengukuran kekristalan dalam polimer.
Kesetimbangan larutan dan perubahan kinetik.
Kesetimbangan protonisasi dan pengompleksan logam.
Derajat dentrasi.
Efek dari asimetri molekular.
Tantomerisasi keto-enol.
Studi struktur alkaloid, steroida, asam lemak dsb.
Studi kinatik untuk rotasi terbatas (restricted rotation) dan isomerisasi.
6. Interpretasi Spektrum.
Langkah-langkah yang perlu diperhatikan adalah :
Jumlah sinyal, menerangkan jumlah proton yang berbeda dalam molekul. Inti yang ekuivalen tidak tidak saling berinteraksi hanya akan menghasilkan satu sinyal.
Kedudukan sinyal, menerangkan lingkungan elektronik setiap macam proton. Semakin kurang inti suatu inti proton tertamengi oleh awan elektron akibat induksi gugus elektronegatif, semakin kearah medan rendah (down field) puncaknya.
Intensitas sinyal, menerangkan berapa banyak proton yang ada pada setiap puncak spektrum. Perbandingan jumlah protonnya sesuai dengan perbandingan tinggi garis integrasinya.
Pemecahan (splitting) sebuah sinyal menjadi beberapa puncak menerangkan jumlah proton tetangganya. Pemecahan oleh n proton yang ekuivalen dari atom yang berdekatan akan menghasilkan ( n + 1 ) puncak. Jika suatu proton (B) dipengaruhi oleh dua kelompok proton tetangga (A dan C) yang tidak ekuivalen maka banyaknya garis B menjadi ( nA + 1 ) ( nC + 1 ), jika nA = proton pada A dan nC = proton pada C.
Konstanta Kopling, makin kecil jika jarak kedua gugus yang berinteraksi makin jauh. Pada jarak 3 ikatan sudah tidak terjadi interaksi lagi. Konstanta Kopling tidak dipengaruhi oleh kuat medan yang dipakai, akan tetapi pergeseran kimia dipengaruhi oleh kuat medan tersebut.
Pustaka :
D.T. Sawyer, W.R. Heineman, and J.M. Beebe; ” Chemistry Experiments for Instrumental Methods”, John Wiley and Sons, New York, 1984, Chap. 11.
R.M. Silverstein, G.C. Basster, and T.C. Morrill; “Spectronic Identification of Organic Compounds”, 4th ed., John Wiley & Sons, New York, 1981, Chap. 4.
D.A. Skoog and D.M. West, ” Principles of Instrumental Analysis “, 2nd ed., Sounders, Philadelphia, 1980, Chap. 14.
─────────────
B. TEKNIK PEMBUATAN SAMPEL
1. Tabung dan Volume Sampel.
Tabung sampel yang digunakan adalah tabung khusus untuk NMR dengan diameter dalam sama dengan 4,000 + 0,01 mm dan panjang 18 mm. Apabila tabung tidak simetris atau mengandung zat asing atau gelembung udara, akan terjadi penurunan daya pisah dan akan menghasilkan “noise”.
Volume sampel yang digunakan untuk pengukuran adalah sekitar 0,4 ml atau kira-kira sampel setinggi 4 cm dari dasar tabung. Apabila volume sampel berlebih, pengukuran tidak akan dipengaruhi, akan tetapi sebaliknya bila sampel terlalu sedikit, daya pisah alat tersebut akan dipengaruhi. Bila titik terendah dari miniskus lebih rendah dari tinggi kumparan RF, posisi sampel akan tidak simetris terhadap kumparan RF dan mengurangi medan magnet akan kurang serangan, dengan demikian akan mempengaruhi resolusi. Lebih lanjut.
Sampel yang digunakan harus sedapat mungkin bebas dari pengotor. Sinyal yang muncul dari zat pengotor dalam sampel kadangkala bertumpangsuh dengan sampelnya sendiri sehingga akan mempersulit interpretasi.
Adanya padatan dalam sampel, termasuk sampel yang tidak larut, akan mempengaruhi daya pisah dan kestabilan daya pisah spektrum, dan jika ada, maka padatan harus dihilangkan atau disaring selama pembuatan sampel.
Adanya zat pengotor paramagnetik dapat memperlebar sinyal NMR. Salah satunya yang paling sering mengotori adalah gas oksigen yang terlarut dalam larutan sampel, maka kadangkala perlu dilakukan “degassing” untuk mendapatkan spektrum dengan resolusi yang baik. Adanya keuntungan dari kekurangan volume untuk resonansi menyebabkan berkurangnya rasio S/N.
Catatan :
Sekalipun volume sampel cukup, harus diperhatikan bahwa titik terendah miniskus tidak dibawah permukaan kumparan pada pemutaran kecepatan tinggi.
Bila volume sampel terlalu sedikit, dapat digunakan tabung mikrosampel yang dapat digunakan untuk sampel sebanyak 0,2 ml.
Sampel gas dapat juga diukur. Bagaimanapun juga, pada tekanan tinggi, perlu dipilih tabung sampel yang sesuai.
2. Cara Penyediaan Sampel.
a. Timbanglah sejumlah tertentu sampel, masukkan ke dalam tabung dan selanjutnya tambahkan pelarut secukupnya. Kocok tabung agar semua sampel larut. Akhirnya tambahkan setengah atau satu tetes standar TMS dan kocoklah.
b. Timbanglah sejumlah tertentu sampel, larutkan dengan pelarut tertentu didalam gelas piala kecil. Pindahkan larutan ke dalam tabung dan selanjutnya tambahkan standar TMS secukupnya.
3. Pelarut dan Konsentrasi Sampel.
Jika sampel yang digunakan berupa padatan atau viskos, pelarut yang cocok sangat dibutuhkan. Pelarut yang ideal adalah pelarut non polar, tidak mengandung proton dan tidak bereaksi dengan sampel. Untuk keperluan ini secara teoritis pelarut yang paling baik adalah CCl4. Akan tetapi ada permasalahan mengenai kelarutan. Dalam beberapa hal CCl4 kurang baik sebagai pelarut, sebagai gantinya yang lebih baik adalah CDCl3. Tetapi harus diperhatikan bahwa pelarut CDCl3 masih mengandung sedikit CHCl3 yang akan memeberikan sinyal pada ppm 7,25 yang juga mungkin merupakan daerah dimana sinyal sampel akan muncul.
Apabila contoh hanya larut dalam air, pilihan yang paling tepat adalah D20 : Tetapi harus diperhatikan bahwa ada kemungkinan reaksi pertukaran antara D dari pelarur H dari pelarut yang mengandung gugus OH atau NH. Bila hal ini terjadi maka puncak OH atau NH dari sampel akan hilang.
Jadi pada hakekatnya, pelarut yang paling baik sangat tergantung pada jenis atau sifat sampel yang diukur.
Konsentrasi sampel dalam larutan sebaiknya cukup tinggi untuk mendapatkan perbandingan S/N yang cukup tinggi. Umumnya untuk senyawa yang menpunyai BM antara 200-500, maka konsentrasi contoh antara 10-20 %. Hal ini tidak selalu berarti bahwa sampel konsentrasi tinggi akan memberikan spektrum lebih baik. Sampel yang mempunyai viskositas tinggi, misalnya, akan memberikan resolusi yang kurang baik. Dalam kasus ini, meskipun sampel berupa larutan, untuk mendapatkan resolusi yang baik perlu dilakukan pengenceran. Pengenceran 50% atau lebih biasanya akan memberikan spektrum yang lebih baik dari sampel murninya.
Pustaka : Instruction JEOL, Sampling Techniques & Spectrum Interprectation of High Resolution NMR.
────────────
- Grass Fire in San Patricio County Fully Contained, But Danger Lingers - April 23, 2026
- Soal HOTS Gerak Dominan Senam PJOK Kelas 6 SD - April 23, 2026
- Chicago Weather: Cold Front Drops Temperatures to 40s with Rain Chances Sunday - April 23, 2026



Leave a Reply