Hukum dan Sifat Sifat Gas
Berikut ialah Poin Poin penting yang perlu dipahami dalam mempelajari Hukum dan Sifat Sifat Gas
Apa itu Gas ?
kumpulan molekul-molekul dengan gerakan kacau balau, acak tapi berkesinambungan kecepatannya bertambah jika temperatur dinaikkan. Molekul-molekul gas terpisah jauh satu sama lain, kecuali selama tabrakan dan bergerak tak bergantungan satu sama lain.
4 Sifat Dasar Untuk Mempelajari gas
- Volume (V)
- Jumlah zat/ jumlah mol (n)
- Tekanan (p)
- Temperatur (T)
- Nilai V, n, p dan T diketahui maka keadaan gas dapat diketahui
- Kapanpun dalam keadaan tsb akan memiliki sifat yang tepat sama (rapatan, kapasitas kalor, warna)
Tekanan
Tekanan adalah Gaya per satuan Luas. Makin besar gaya yang bekerja pada permukaan tertentu, makin besar tekanannya. Satuan SI tekanan adalah pascal (Pa), namun adapula satuan lainnya, yaitu bar dan atmosfer (atm).
Temperatur
Temperatur ialah sifat yang menunjukkan Arah Energi.


Hukum Ke Nol Termodinamika
“Jika A dalam keseimbangan termal dengan B dan B dalam keseimbangan termal dengan C, maka C juga dalam keseimbangan termal dengan A. “
Hukum Hukum Gas
- Boyle
- Gay Lussac
- Avogadro
- Dalton
Gas Ideal
Gas yang mematuhi persamaan (1) secara tepat di sebut gas sempurna atau gas ideal.
Besar nilai R sama untuk setiap gas yaitu: 8,314 JK-1
1.Hukum Boyle
Respons terhadap tekanan temperatur tetap,
volume sejumlah tertentu gas berbanding terbalik dengan tekanannya.
2.Hukum Gay Lussac
menaikkan temperatur gas akan menambah kecepatan rata-rata molekulnya
3.Hukum Avogadro
yaitu volume yang sama dari gas pada tekanan dan temperatur sama mengandung jumlah molekul yang sama.
Vm = V/n
Vm=RT/p
4.Hukum Dalton
Sekanan yang dilakukan oleh campuran gas sempurna adalah jumlah tekanan yang dilakukan oleh masing-masing gas tersebut yang secara sendiri menempati volume yang sama.
p = pA + pB + pC + … = ∑J p J
Interaksi Moleular Gas
Gas nyata menunjukan menunjukan penyimpangan dari hukum gas ideal karena molekul-molekulnya berinteraksi. Gaya tolak-menolak antar molekul membantu ekspansi dan kompresi. Interaksi molekular:
a. Faktor pemampatan
b. Koefisien virial
c. Pengembunan
d. konstanta kritis
A.Faktor Pemampatan
Gas nyata yang memperlihatkan ketergantungan gaya terhadap jarak dapat diperagakan antara faktor pemampatan Z, dengan:
Z = P.Vm/RT
Pada tekanan tinggi semua gas mempunyai Z>1 menunjukkan gas-gas itu sulit dimampatkan dari pada gas sempurna.
B. Koefisien Virial
Rumus diatas adalah persamaan keadaan virial (nama ini berasal dari bahasa latin untuk gaya).
Koefisien virial yang ketiga biasanya kurang penting dari kedua artinya : C/V2m << B/Vm
Persamaan virial dapat digunakan memeragakan persamaan keadaan gas nyata dapat sama dengan gas sempurna sewaktu P, semua sifat-sifatnya tidak perlu sama dengan sifat-sifat gas sempurna.
Faktor pemampatan, untuk gas nyata: dz/dp = B + 2pC + . . .
B’ tidak pernah nol oleh karena itu untuk gas nyata Z ketika P kemiringan kurva Z terhadap p tidak mendekati nol.
Karena koefisien virial bergantung pada temperature, mungkin ada temperatur dimana Z mendekati 1 dengan kemiringan kurva nol adalah tekanan rendah / volume molar tinggi.
C. Pengembunan
Apabila keadaan tekanan, suhu, dan volume gas dapat diatur sehingga gaya tarik-menarik maksimum ini dapat dicapai, gas akan mulai berubah menjadi cairan.
Persamaan Van Der Walls
Interaksi tolak-menolak molekuler diasumsikan bahwa interaksi itu menyebabkan molekul-molekul berprilaku sebagai bola kecil tetapi tidak dapat ditembus.
Volume bukan-nol molekul menyiratkan bahwa partikel itu tidak bergerak dalam volume V, tetapi terkekang di dalam volume yang lebih kecil yaitu V-nb. Dengan nb adalah perkiraan volume total yang ditempati molekul-molekul itu sendiri.
P = nRT/V –> P = (nRT)/(V-nb)
Tekanan bergantung baik pada frekuensi tabrakan dengan dinding maupun pada gaya setiap tabrakan berkurang akibat gaya tarik. Akibatnya persamaan vand er wallsnya:
Persamaan ini sering ditulis dalam istilah volume molar Vm2= V/n sebagai
Istilah a/Vm disebut tekanan internal gas. Persamaan Van der Waals ditulis dalam bentuk persamaan gas akan menjadi :
Ciri-ciri utama persamaan Van der Waals:
Isoterm gas sempurna diperoleh pada temperature tinggi dan volume molar besar
Cairan dengan gas berada bersama-sama jika efek kohesi dan disperse berada dalam keseimbangan
Konstanta kritis berhubungan dengan koefisien-koefisien Van der Waals
Temperatur Boyle berhubungan dengan temperature kritis
Gas nyata berbeda dengan gas sempurna dimana gas nyata tidak mematuhi hukum gas ideal. Deviasi yang terjadi di dalam gas nyata akan mempengaruhi mudah atau sulitnya gas tersebut untuk digunakan. Di dalam gas nyata terdapat interaksi molekuler yang terdiri atas gaya repulsif dan gaya atraktif
Gaya repulsif merupakan gaya yang ada ketika gas mengalami kompresi dimana pada saat pengompresian volume akan berkurang dan atom atom akan saling tolak menolak , semakin besar gaya repulsif suatu senyawa gas maka akan sulit untuk ditekan.
Gaya atraktif merupakan kebalikan dari gaya repulsif dimana semakin banyak elekton yang berinteraksi akan menyebabkan substansi tetap dalam fase gas, dimana atom atom akan saling tarik menarik.
Diagram yang terbentuk akibat gaya atraktif dan repulsif
Semakin kecil deviasi yang dimiliki oleh gas nyata maka semakin mendekati sifat gas ideal yang menyebabkan gas tersebut berubah fasa dengan penurunan temperatur, maupun peningkatan tekanan. Besar kecilnya deviasi ditentukan dengan rumus :
Z = PVmolar/RT
Penentuan Z , yaitu :
Z = 1 ( merupakan gas ideal )
Z > 1 ( tekanan diturunkan , maka gaya repulsif mendominasi , gas mendekati titik kritis )
Z< 1 ( terjadi pada tekanan tinggi ketika molekul bertumbukan , gaya atraktif mengambil alih)
Semakin besar Z, lebih sulit dimampatkan.
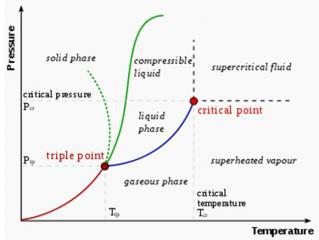
Dengan adanya titik kritis dan titik tripel maka berakibat tiap molekul dapat dirubah menjadi fasa gas dan fasa cairan , mudah atau tidaknya senyawa berubah fasa dipengaruhi oleh gaya interaksi molekuler yang ada di dalamnya.
Grafik yang didapat menjadi :
Dalam gas nyata terdapat faktor penyesuaian yang disebut dengan koefisien virial yang dinyatakan dalam
Perhitungan dalam gas nyata melalui perhitungan Van Der Walls dengan faktor koreksi yang ada , maka hal ini menjadi
Pengamatan pengamatan yang mewujudkan gas gas nyata pada T dan V sama melakukan tekanan tereduksi yang sama , dan terjadi pada molekul polar pada kondisi
Tekanan tereduksi : Pr = P/Pc
Volume tereduksi : Vr = V/Vc
Temperatur tereduksi : Tr = T/Tc
- Latihan Soal OSN Ilmu Komputer SMA 2026 - June 1, 2026
- Latihan Soal OSN Kebumian SMA 2026 - May 31, 2026
- Latihan Soal OSN Geografi SMA 2026 - May 30, 2026
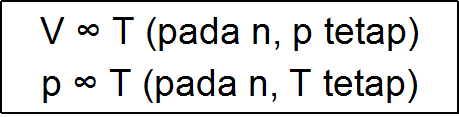

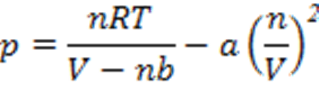
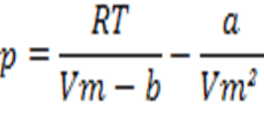
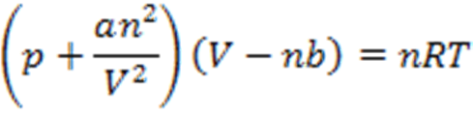






Leave a Reply