Menghitung Konsentrasi Suatu Zat
Konsentrasi dapat diartikan sebagai ukuran yang menentukan banyaknya zat yang berada di dalam suatu campuran dan dibagi dengan volume total pada campuran tersebut. Biasanya konsentrasi dinyatakan pada satuan fisik, seperti halnya satuan volume, satuan kimia, ataupun satuan berat seperti mol, ekuivalen dan massa rumus. Pada bahasan ini, kita akan Menghitung Konsentrasi Suatu Zat dan memahami bagaimana konsentrasi berhubungan dengan persen konsentrasi, PPM (Parts per Million) atau PPB (Parts per Billion), fraksi mol, molaritas, dan molalitas.
1. Persen konsentrasi
Pada umumnya di bidan kimia, persen digunakan untuk menyatakan konsentrasi suatu larutan. Persen konsentrasi dapat dibagi menjadi persen volume dan persen berat.
Untuk mengukur persen berat (%W/W) menggunakan rumus :
Sedangkan untuk mengukur persen volume (%V/V) menggunakan rumus :
![]()
(Baca juga artikel Cara mengencerkan larutan )
2. PPM (Parts per Million) dan PPB (Parts per Billion)
Untuk yang ini biasanya digunakan pada larutan yang sangat enver dengan satuan PPB dan PPM. Satuan PPM ekuivalen dengan 1 mg zat terlarut dalam 1 liter larutan, sedangkan PPB ekuivalen dengan 1 ug zat terlarut per 1 liter larutan.
PPM dan PPB memang merupakan satuan yang mirip seperti persen berat. Jika persen berat, gram zat terlarut per 100 gram larutan, maka PPM gram teralrut per satu juta gram larutan, serta PPB zat terlarut per miliar gram larutan.
3. Fraksi Mol (X)
Fraksi mol merupakan perbandingan mol salah satu komponen degnan jumlah mol dari seluruh komponen. Bila suatu larutan mengandung zat P dan Q dengan jumlah mol masing-masing nP dan nQ, maka rumus untuk menentukan fraksi mol pada tiap komponen adalah :
Untuk melihat cara Bagian Molaritas dan Molalitas bisa lanjut ke halaman 2
Halaman 1 2
- Grass Fire in San Patricio County Fully Contained, But Danger Lingers - April 23, 2026
- Soal HOTS Gerak Dominan Senam PJOK Kelas 6 SD - April 23, 2026
- Chicago Weather: Cold Front Drops Temperatures to 40s with Rain Chances Sunday - April 23, 2026


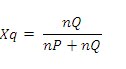



72 comments