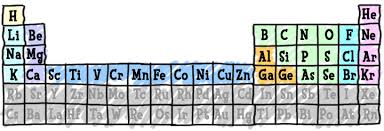
Golongan sistem periodik
Tahukah kalian unsur-unsur dalam satu golongan bisa jadi memiliki kemiripan sifat? Hanya saja mungkin kadarnya yang berbeda.
Contohnya salah satu sifat unsur logam alkali (golongan IA) yaitu bereaksi dengan air. Akan tetapi kecepatan reaksinya berbeda. Dari atas ke bawah, unsur-unsur itu bereaksi makin dahsyat.
Satu hal yang harus disadari bahwa setiap unsur mempunyai sifat khas yang membedakan dan unsur lainnya. Pengelompokkan unsur dalam satu golongan dapat dibandingkan dengan pengelompokkan makhluk hidup.
Yuk kita lihat kemiripan sifat diantara unsur segolongan pada beberapa golongan berikut.
1. Golongan VIIIA (Gas Mulia)
Unsur-unsur golongan VIII A yaitu helium, neon argon, kripton, xenon, dan radon disebut gas mulia karena semuanya berupa gas yang sangat stabil, sangat sukar bereaksi dengan unsur lain. Unsur gas mulia terdapat di alam sebagai gas monoatomik (atom-atomnya berdiri sendiri). Menurut para ahli, hal itu disebabkan kulit terluarnya yang sudah terisi penuh. Kulit terluar yang sudah penuh, menjadikan unsur tidak reaktif.
2. Golongan VIIA (Halogen)
Unsur- unsur golongan VIIA merupakan kelompok unsur nonlogam yang sangat reaktif. Semua unsur halogen bereaksi dengan tipe yang sama, walaupun kereaktifannya berbeda. Halogen dengan logam membentuk senyawa yang kita sebut garam. Contohnya NaF, NaCl, NaBr, dan NaI. Oleh karena itu pula unsur golongan VIIA disebut halogen yang artinya pembentuk garam. Kereaktifan unsur halogen berkurang dari F ke I. Semua unsur halogen (golongan VIIA) yang beru pa molekul diatomik (F2, Cl2, Br2, I2) berwarna dan bersifat racun. Fluorin berwarna kuning muda, klorin berwarna hijau muda, bromin berwarna merah, dan uap iodin berwarna ungu.
3. Golongan IA (Logam Alkali)
Unsur- unsur golongan IA, kecuali hidrogen disebut logam alkali karena golongan tersebut membentuk basa yang larut dalam air. Semua logam alkali tergolong logam yang lunak (kira-kira sekeras karet penghapus) dan ringan (massa jenis Li, Na, dan K kurang dari 1 gram cm^-3. Logam alkali mempunyai 1 elektron valensi yang mudah leas sehingga merupakan kelompok logam yang paling aktif, dapat terbakar di udara, dan bereaksi hebat dengan air. Kereaktifan logam alkali bertambah dari litium ke fransium.(Baca juga Pembahasan Golongan Unsur ALKALI (IA))
4. Golongan IIA ( Logam Alkali Tanah)
Unsur-unsur golongan IIA disebut logam alkali tanah karena dapat membentuk basa, tetapi senyawa-senyawanya kurang larut dalam air. Unsur alkali tanah umumnya ditemukan dalam bentuk senyawa berupa deposit (endapan) dalam tanah. Logam alkali tanah juga tergolong logam aktif, tetapi kerekatifannya kurang dibandingkan dengan logam alkali seperiode, dan hanya akan terbakar di udara bila dipanaskan.
5. Unsur-unsur Transisi
Unsur-unsur transisi adalah unsur yang terdapat di bagian tengah sistem periodik, yaitu unsur-unsur golongan tambahan (golongan B). Unsur-unsur transisi mempunyai sifat-sifat khas yang membedakannya dari unsur golongan utama, diantaranya:
* Semua unsur transisi tergolong logam
* Mempunyai kekerasan, titik leleh, dan titik didih yang relatif tinggi
* Banyak diantaranya membentuk senyawa-senyawa berwarna
- Latihan Soal OSN Geografi SMA 2026 - May 30, 2026
- Latihan Soal OSN Ekonomi SMA 2026 - May 29, 2026
- Latihan Soal OSN Astronomi SMA 2026 - May 28, 2026



Leave a Reply