Kimia : Ilmu pengetahuan yang mempelajari tentang materi meliputi susunan, struktur, sifat dan perubahan materi serta energi yang menyertainya.
Materi : segala sesuatu yang mempunyai massa dan yang mempunyai volume (menempati ruang).
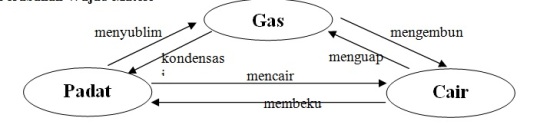
Materi mempunyai 3 wujud : padat (solid), cair (liquid/aqueous) dan gas (gas).
Perubahan wujud materi : materi yang berubah dari 1 wujud ke wujud lain.
| Sifat | Perubahan Fisika | Perubahan Kimia |
| Hasil materi baruWujudCiri-ciri | tidak menghasilkanberubahhanya melibatkan perubahan wujud, tetapi tidak menghasilkan materi baru | menghasilkanberubahmenghasilkan materi baru, ditandai adanya pembentukan gas, pembentukan endapan, perubahan warna, dan perubahan suhu |
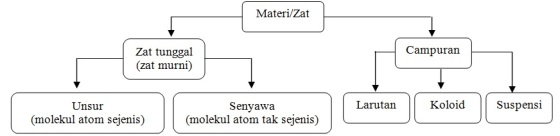
Materi digolongkan :
- Unsur : zat yang tidak bisa diuraikan ke bentuk sederhana melalui reaksi kimia.
- Senyawa : zat yang terbentuk oleh 2 unsur / lebih unsur yang berbeda, dengan komposisi tetap.
- Campuran : zat yang terbentuk oleh banyak unsur dengan komposisi tak tetap
| Pengolongan Campuran | Definisi |
| Larutan
Koloid
Suspensi |
Campuran homogen antara dua zat / lebih dimana partikel2 komponen2 penyusunnya tersebar secara merata, terdiri atas pelarut dan zat terlarut.Campuran heterogen antara 2 zat atau lebih dimana partikel2 zat yang berukuran koloid (fase terdispersi) tersebar secara merata dalam zat lain (fase pendispersi).
Campuran heterogen antara 2 zat atau lebih yang berukuran suspensi. |
| Pemisahan | Metode yang digunakan |
| zat padat dari zat padat lainnyazat padat dari zat cair dalam larutanzat padat dari zat cair dalam suspensi
beberapa zat padat dari campuran zat-zat cair yang tidak saling melarutkan zat cair dari larutannya |
pengayakan, pemisah magnetik, pelarutanpenguapan / evaporasi, kristalisasipenyaringan / filtrasi, sentrifugasi
kromatografi corong pisah destilasi / penyulingan, destilasi bertingkat |
Kadar zat dalam campuran biasanya dinyatakan sebagai perbandingan jumlah zat dengan jumlah campurannya dalam bagian perseratus (%) atau bagian perjuta (bpj) atau ppm (part permillion).
| 1 bagian = 106 ppm (bpj) 1 % = 104 ppm (bpj) |
Satuan kadar zat dapat dinyatakan dalam perbandingan massa atau volume, yaitu persen (%) massa, persen (%) volume, bpj (ppm) massa, dan bpj (ppm) volume.
- Klasifikasi Materi
|
| – komposisinya tidak tetap- dapat dipisahkan menjadi zat asalnya melalui cara-cara fisika, seperti dengan penyaringan |
|
- Partikel Materi
Materi tersusun atas partikel-partikel yang dapat berbentuk atom, molekul, atau ion.
- Atom : partikel terkecil dari suatu unsur yang masih mempunyai sifat-sifat unsur itu
- Molekul : gabungan dua atau lebih atom yang sama atau berbeda
- Ion : atom atau kumpulan atom yang bermuatan listrik
Contoh : Na+, Al+3 (kation) atau Cl–, SO4-2 (anion)
- Sifat Materi
- Sifat fisika : sifat yang dapat diamati tanpa mengubah susunan materi
- Sifat kimia : sifat yang dapat diamati akibat terjadi perubahan materi menjadi materi lain
Atau :
- Sifat ekstensif : sifat yang dipengaruhi oleh jumlah zat
Contoh : massa, volume, dan kandungan energi (entalpi)
- Sifat intensif : sifat yang tidak dipengaruhi oleh kuantitas/jumlah materi
Contoh : warna, bau, rasa, dan titik lebur
- Perubahan Materi
- Perubahan fisika : tidak menghasilkan zat baru, hanya melibatkan perubahan bentuk atau wujud zat à campuran
Contoh : beras menjadi nasi, lilin meleleh
- Perubahan kimia : menghasilkan materi baru yang berbeda sifatnya dengan materi asalnya → senyawa. (Yang menyertai perubahan kimia : pembentukan gas, endapan, warna, atau suhu)
Contoh : fotosintesis, telur membusuk
Perubahan Wujud Materi
Sebagian besar materi di alam berada sebagai campuran zat-zat murni. Untuk memperoleh zat murni tersebut, beberapa pemisahan campuran yang dapat dikelompokkan menjadi beberapa jenis :
Pemisahan zat padat dari suatu suspensi
Suatu suspensi dapat dipisahkan dengan metode Penyaringan / Filtarsi dan metode Sentrifugasi / Centrifuge.
- Pada metode filtrasi hasilnya disebut filtrat (bagian yang jernih) dan sisanya disebut residu (bagian padat)
- Pada metode Sentrifugasi, dilakukan pemusingan, sehingga terjadi pengendapan / sedimentasi lalu didekantasi / dituang atau dipipet secara hati-hati sehingga didapat zat padatnya.
Pemisahan zat padat dari larutan
Zat padat yang terlarut dapat dipisahkan dengan metode penguapan / evaporasi dan kristalisasi.
Penguapan
|
Kristalisasi
|
- Pemisahan campuran zat cair
Zat cair dapat dipisahkan dengan metode distilasi (penyulingan), metode distilasi bertingkat, dan metode corong pisah.
- Corong pisah digunakan untuk memisahkan cairan yang tidak saling melarutkan, contohnya campuran air dan minyak.
- Distilasi bertingkat : proses distilasi berulang-ulang dan adanya kolom fraksionasi yang terdiri atas beberapa plat yang bertindak sebagai tempat pengembunan. Destilasi ini digunakan pada pemisahan zat cair yang sama-sama mudah menguap. Contohnya pemurnian minyak bumi, yaitu memisahkan gas, bensin, minyak tanah dan sebagainya
- Distilasi : suatu proses penguapan yang diikuti pengembunan, contohnya pengolahan air tawar dari air laut.
Kromatografi
Cara pemisahan komponen-komponen yang terdiri dari 2 fase : fase mobil (fase bergerak) dan fase stasioner (tetap). Berdasarkan perbedaan terikatnya suatu komponen pada fase stasioner dan perbedaan kelarutannya fase mobil. Komponen yang kurang larut dalam fase mobil atau yang lebih kuat terjerap (teradsorpsi) pada fase stasioner akan tertinggal, sedangkan komponen yang lebih larut atau kurang terjerap akan bergerak lebih cepat.
- Macam kromatografi : K. Kertas dan K. gas
- Contohnya : pemisahan campuran zat warna, memisahkan komponen monosakarida pada polisakarida.
Pemisahan dua jenis padatan
- Sublimasi
- Didasarkan atas kemudahan zat untuk menyublim atau tidak
- Campuran dipanaskan secara perlahan, dan zat yang mudah menyublim akan menyublim terlebih dahulu. Uap yang terbentuk, kemudian didinginkan sehingga akan menghablur kembali.
- Contoh : pemisahan iodin, kapur barus dari campurannya.
2. Kristalisasi
- Didasarkan atas perbedaan kelarutan dari komponen campuran dalam pelarut tertentu.
- Makin tinggi suhu, makin besar kelarutan. Serta, komponen yang berbeda dalamsutua campuran akan melarut dalam pelarut yang berbeda pula.
- Contoh : pemisahan KNO3 dan NaNO3 yang memiliki kelarutan pada suhu yang berbeda
REFERENSI
Tim Grasindo. Top no.1 Pendalaman Materi Kimia SMA Kelas X,XI,XII . 2014 . Grasindo : Jakarta





Terima kasih atas isi dari web yang sangat baik.
Apa saya bisa tahu referensi dari isi halaman ini? Terima kasih.
Coba pak nanti saya cari tau dlu. agak lupa juga
Ok. Saya tunggu balasannya. Terima kasih.
Saya lupa beri referansi di artikelnya, sekarang sudah saya tambahkan pak
[…] sumber : bisakimia […]