pH larutan penyangga
1. Sistem penyangga asam dengan basa konjugasinya
- Disebut juga buffer asam
- Buffer asam → asam lemah + basa konjugasinya
- Harga pH lebih kecil dari 7 (pH < 7)
- Tergantung dari harga Ka asam lemah dan perbandingan mol asam lemah (nA) dan mol basa konjugasinya (nG).
Contoh :
Hitung pH larutan penyangga yang dibuat dari 100 mL larutan CH3COOH 0,1 M dengan 200 mL CH3COONa 0,1 M (Ka CH3COOH = 105)
Jawab :
CH3COOH = 100 mL x 0,1 mol L-1 = 10 mmol (asam)
CH3COONa = 200 mL x 0,1 mol L-1 = 20 mmol (basa konjugat)
2. Sistem penyangga basa dengan asam konjugasinya
- Disebut juga buffer basa
- Buffer basa → basa lemah + asam konjugasinya
- Harga pH lebih besar dari 7 (pH > 7)
- Tergantung dari harga Kb pada basa lemah dan perbandingan mol basa lemah (nB) serta mol asam konjugasinya (nG)
Contoh :
Dalam 1 liter larutan terdapat 0,01 mol NH3 dan 0,02 mol NH4+ yang berasal dari kristal (NH4)SO4. Jika Kb NH3 = 10-5, maka berapa pH larutan tersebut?
Jawab :
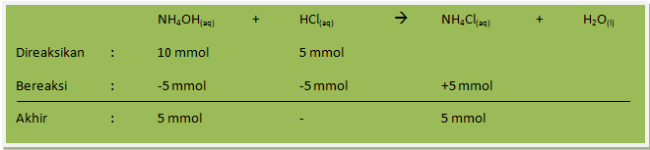
Hitung pH larutan yang dibuat dari campuran 100 mL larutan NH4OH 0,1 M dengan 50 mL larutan HCl 0,1 M (Kb NH4OH = 10-5)
Jawab :
NH4OH = 100 mL x 0,1 mol L-1 = 10 mmol
HCl = 50 mL x 0,1 mol L-1 = 5 mmol
Sumber : Modul Kimia kelas XI
Untuk artikel sebelumnya yaitu larutan penyangga part 1. silahkan klik disini

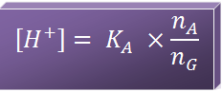

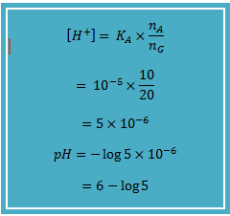
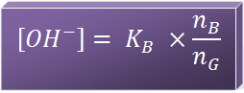
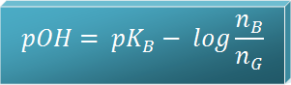

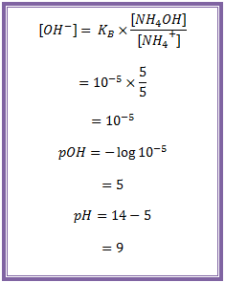



[…] Editor’s note: artikel ini merupakan lanjutan dari bagian 1 dan bagian 2. […]
contoh soal studi kasus larutan buffer ada gak??
[…] ini adalah contoh soal dan pembahasan Larutan Penyangga. Jika kalian sudah membaca materi tentang Larutan Penyangga, salah satu cara untuk lebih memahami materi pelajaran tersebut adalah dengan mengerjakan soal-soal […]